CIRUGIA DEL SENO FRONTAL
Cirugía del seno frontal – Urquiola Federico Adolfo – 2006
Objetivos
– Describir la compleja anatomía del seno frontal, tanto en su configuración externa como en su intrincado sistema de drenaje.
– Investigar la historia de la cirugía del seno frontal analizando su evolución en el transcurso del tiempo.
– Desarrollar los actuales abordajes al seno frontal, sus indicaciones y la técnica quirúrgica de cada uno.
Introducción
El seno frontal (SF) es considerada un área quirúrgica difícil y de grandes controversias sobretodo al hablar de buenos resultados a largo plazo y de complicaciones postoperatorias (1). Es un seno particularmente complejo dada la necesidad de preservar el conducto nasofrontal.
Tiene especial interés la patología que involucra a este seno y la rica historia acerca de los distintos procedimientos empleados para el tratamiento de estas enfermedades que incluye a importantes profesores argentinos.
La cirugía frontal como tal existe hace 115 años y el concepto de receso frontal como vía de drenaje del SF fue introducido por Killian en 1896, de allí en adelnate se desenvolvieron distintas escuelas y pensamientos referentes al mejor tratamiento de la patología frontal y discusiones acerca de la vía de abordaje externa versus la intranasal (1). Actualmente el avance de la tecnología abrió un gran portón de alternativas quirúrgicas mínimamente invasivas para el paciente con enfermedad en el SF.
En esta monografía se hará un desarrollo de la historia de la cirugía frontal como también de las alternativas quirúrgicas que se encuentran hoy día disponible haciendo hincapié en la compleja anatomía que involucra este controvertido seno paranasal.
Historia de la cirugía del seno frontal
Vesalius describió por primera vez los senos frontales, maxilares y el seno esfenoidal. Poco o ningún progreso ocurrieron en los miles de años subsiguientes (1). Hasta que en 1704, Lettre desarrolló la trepanación del SF. Sin embargo, no ocurrió ningún desarrollo en el diagnóstico y tratamiento de la patología del SF hasta finales del siglo XIX cuando en 1884 Ogston operó por primera vez el SF (1).
Históricamente, las primeras cirugías del SF eran muy radicales, con remoción parcial o total de la pared anterior del seno cuya consecuencia era una deformación cosmética importante. Luego siguió una era de cirugía intranasal que trajo diversos fracasos con una alta morbilidad y alta mortalidad. En 1905, Fletcher Ingals describe el uso de una “spring-gold tube” para stent del conducto nasofrontal que quedaba en posición por 3 a 4 meses. Su artículo fue publicado en 1917 donde describe que la paciente irrigaba su propio seno y que obtenía tal alivio que no quizo retirarse la sonda hasta los pasados 3 años y medio. Sin embargo, estos procedimientos intranasales no obtuvieron una preferencia entre los otorrinolaringólogos de aquella época (1).
En 1921 se introduce el procedimiento de Lynch, sin embargo, las obstrucciones del ducto nasofrontal llevaron a 20 al 33% de fracasos. Le siguieron modificaciones a esta técnica como la de Sewell-Boyden y la de Neel. A finales del 1800 se describe la cirugía osteoplástica con obliteración de grasa por sinusitis crónica. Esta técnica se ha popularizado a partir del 1958 y hoy en día es utilizada en varios centros otorrinolaringológicos (2).
Actualmente, los avances tecnológicos trajeron a la cirugía endoscópica transnasal y a medida que avanzó la experiencia con este abordaje en los distintos senos paranasales el interés en el seno frontal ganó lugar basándose en la mejoría de permeabilidad de receso frontal.
Desarrollo embriológico
Este desarrollo está basado en los estudios de Schaeffer y Kasper que describen la existencia de 4 depresiones o surcos frontales sobre la pared lateral superior del meato medio embriológico. Estos 4 surcos se diferencian en varias celdillas etmoidales anteriores. El SF se desarrolla a partir de la evaginación de un segundo surco frontal que crece a partir de una región etmoidal anterior para el interior del hueso frontal. De aquí se deduce que el SF es embriológicamente una celdilla etmoidal. Las células del receso frontal se desarrollan a medida que las 4 depresiones invaden las paredes de dicho receso distorcionando el drenaje del seno. La conexión nasofrontal se vuelve tortuosa (1). Se deduce entonces que la neumatización del hueso frontal se realiza a partir del receso frontal (Killian) (5).
Esta descripto que la primera depresión frontal generalmente se diferencia en la primera célula de la eminencia nasal o agger nasi, la segunda en células del seno frontal y la tercera y cuarta en celdillas etmoidales anteriores. La bulla etmoidal se desarrolla a partir del segundo etmoturbinado y no de las depresiones frontales.
Anatomía del seno frontal
El SF es una estructura par que se desarrolla aproximadamente en el duodécimo año de vida. Según Wolf, este desarrollo puede ocurrir a los 7 años de vida y no pueden reconocerse por las imágenes antes de los 6 años (1). Puede existir un seno muy desarrollado, pobremente desarrollado y no son infrecuentes las agenesias de uno o ambos senos (5% de la población) (3). Es por ello que son considerados los senos más variables y serían como las huellas digitales. Una celdilla etmoidal excesivamente neumatizada puede reemplazar a este seno.
El seno frontal es una celdilla etmoideofrontal y tiene la forma de una pirámide triangular de base inferior y 2 cm. de altura en promedio. Se describen 3 paredes, una base y un vértice. La pared anterior corresponde a la región supraorbitaria y su espesor es de 3 o 4 mm. La pared posterior se relaciona con la meninges y el encéfalo y solo mide 1 mm. La tercera pared es la interna. La base tiene dos partes: una externa u orbitaria y otra interna o etmoidal (4) (fig.1)
Las dimensiones del SF son variables. Se llama senos pequeños a aquellos cuya cavidad no tiene relación con la parte vertical del frontal y corresponde solamente al ángulo superointerno de la cavidad orbitaria. Según Rouvière en el 12% encontramos este caso (4). Pueden observarse distintas variaciones anatómicas como senos supernumerarios o tabicamientos incompletos (3).
Cuando la terminación anterior de la fosa olfatoria protruye hacia el seno frontal, se habla de seno frontal peligroso. Draf indicó que el área superior del septum del seno frontal se encuentra frecuentemente desplazada de la línea media, mientras que las inferiores no. El SF neumatiza la crista galli en un 10% (8).
El SF está irrigado por la arteria supraorbitaria y la arteria etmoidal anterior. La inervación la provee el nervio supraorbitario que es rama del nervio oftálmico (V1). El drenaje venoso es clínicamente importante porque llega al seno sagital superior y al esfenoparietal por medio de los vasos supraorbitario y oftálmico superior junto con el drenaje de las venas diploideas (3).
La abertura del seno frontal se denomina ostium frontal interno conectado al seno etmoidal anterior. Está claramente demostrado que el SF drena a través de un espacio ocupado por las celdillas etmoidales anteriores y no a través de un ducto o conducto como se creía anteriormente y es mejor utilizar el término receso para este espacio (1) (Fig.1). Queda conformado un reloj de arena entre el seno frontal y el receso siendo su parte estrecha el ostium frontal y el receso se abriría hacia abajo como si fuera un embudo. Según Kuhn, el receso frontal es un espacio potencial, neumatizado por una o más celdillas etmoidales (células del receso frontal) y una pequeña cantidad de edema puede obstruir este espacio y por lo tanto obstruir el drenaje del SF (1).
Anatomía endoscópica del seno frontal
Killian fue el primero en 1896 en utilizar el término receso frontal (1). El receso frontal es quizá la estructura más complicada del complejo etmoidal anterior. La pared medial del receso es la parte más anterior y superior del cornete medio. La pared lateral es mayormente la lámina papirácea (6) (fig.2). Este receso que es por donde drena el SF está ubicado en la porción más superior del meato medio justo detrás de la inseción anterior del cornete medio en la pared lateral nasal. Por debajo dicho receso se abre dentro del infundíbulo etmoidal (22).
En 1941, Van Alyea estudió el receso en 247 disecciones. Describió varias celdillas etmoidales anteriores que neumatizaban la región y advirtió que tenían potencial para obstruir el receso contribuyendo o incluso causando una sinusitis frontal. Estas celdillas influencian claramente en el drenaje del SF y la remoción inadecuada puede llevar al fracaso quirúrgico (fig.3 y 4). Al referirnos acerca de celdillas etmoidales anteriores significa que involucra a la celdilla de agger nasi, celdillas frontales, celdillas etmoidales supraorbitarias, celdillas septales del seno interfrontal, celdillas suprabulares y celdillas infundibulares. Las tres primeras son las más importantes y responsables de los problemas del receso frontal (1).
Agger significa en latín cresta o montículo, ubicado en este caso en la pared lateral, encima y ligeramente anterior al origen del cornete medio. Esta área puede neumatizarse. Bolger, en una revisión de más de 200 imágenes de TC constató la presencia en el 98,5% de los pacientes. Es la célula más anterior y más constante del receso frontal (1).
Wormald propone que el agger nasi es la llave para comprender la compleja área que resulta ser el receso frontal. Concluye que la anatomía y las variaciones anatómicas comunes que ocurren en este receso son pobremente comprendidas por los cirujanos rinosinusales. Aclara que los cortes finos de TC coronales y parasagitales (Fig.5) ayudan a la identificación de cada celdilla individual y permiten al cirujano formular un plan quirúrgico preciso y claro (7).
Las paredes medial y posterior son las dos únicas independientes y no forman parte del cráneo pudiendo ser removidas.
Las células frontales se dividen en 4 variantes siempre en conjunto con la célula de la eminencia nasal (Tabla I). Células frontales tipo I consiste en una célula única en el receso frontal encima de la célula de la eminencia nasal, tipo II: una serie de de dos o más celdillas frontales encima de la eminencia nasal, tipo III: una celdilla maciza que se extiende del meato medio para dentro del seno frontal y tipo IV: celdilla aislada dentro del seno frontal. Las celdillas frontales nacen un poco más posterior que la eminencia nasal. Las celdillas tipo IV puede cerrar totalmente el ostium frontal y da el aspecto de una bola de aire dentro de un seno opaco (Fig.6).
La celdilla etmoidal supraorbitaria se desarrolla posterior a la eminencia nasal, la celdilla frontal y el seno frontal. Generalmente se localiza en la bulla etmoidal. Esta celdilla se extiende sobre la órbita y una dos o más de estas celdillas pueden existir en el receso frontal. Debe existir la sospecha de la presencia de esta celdilla cuando en la TC se observa la neumatización del SF fuera y encima de la órbita. Un seno frontal tabicado es también una característica de una celdilla etmoidal supraorbitaria con neumatización extensa.
También se describen una celdilla septal del seno interfrontal que ocurre en el septo entre los dos senos frontales. puede irse al techo e incluso comunicarse con una neumatizada apófisis crista galli. El ostium puede hallarse medial y anterior al ostium frontal o algunas veces puede abrirse dentro del SF (1). La celdilla suprabullar ocurre en la lamela de la bulla etmoidal, encima de esta bulla y cierra el receso por detrás. Encontrarla y removerla endoscópicamente es muy dificultoso. Celdilla de la bulla frontal no es muy conocida. Su origen y localización son variables y por lo tanto no se cree que exista como tal sino que sería un SF poco desarrollado.
Existen 3 configuraciones básicas de la apófisis unciforme (Fig.7). Puede extenderse directamente en dirección superior e insertarse en la base de cráneo. La segunda confiruración consiste en la curvación medial e inserción en el cornete medio. Por último, puede insertarse en la lámina papirácea produciendo el llamado receso terminalis (5). El receso terminalis se forma cuando el proceso unciforme se inserta en la pared medial de la órbita, haciendo que el infundíbulo etmoidal termine en un saco ciego. El SF drena medialmente a la unciforme directamente dentro del meato medio y no en el infundíbulo etmoidal como lo hace habitualmente (1).
En la figura 8 puede observarse un diagrama que grafica las diferentes formas en las que el agger nasi, la apófisis unciforme y la bulla etmoidal estrechan el receso frontal.
Fisiología
Messerklinger describió los patrones de limpieza mucociliar de los senos paranasales y abrió un camino para la comprensión de la fisiología de este particular seno. El patrón mucociliar se eleva para el septo del seno interfrontal, en sentido lateral, a través del techo del seno y luego a su pared lateral y luego medial hasta su drenaje a través del ostium (Fig.9). También está descripto que una parte del moco que se dirige hacia abajo da la vuelta y vuelve al seno frontal cerrando de esta manera el circuito. Solamente una porción del moco sale en un pasaje en cuanto que el resto recircula. Es factible que cuando el moco se encuentra en el receso frontal pueda capturar material extraño como bacterias u hongos que pueden ser llevados dentro del seno (1).
El receso frontal puede ser influenciado y estrechado por diversos factores anatómicos como ser el proceso uncinado, células agger nasi, bulla etmoidal u otras celdillas etmoidales. Muchas veces existen combinaciones de estos factores en aquellos pacientes que sufren sinusitis aguda o crónica. Estas estructuras estrechan la parte inferior del “reloj de arena” descripto anteriormente y al empujar el receso desde detrás dan la falsa idea de “conducto nasofrontal” como se lo denominaba anteriormente (5).
Es por ello que diversos autores consideran a la restauración de la función del receso frontal como el principal objetivo en el tratamiento de la patología inflamatoria frontal (1).
Evolución histórica de los abordajes al seno frontal
En 1954 MacBeth estableción que el tratamiento de la sinusitis frontal crónica es uno de los temas más insatisfactorios para la rinología. Hoy día este concepto continua vigente (12).
En 1870 fue publicado el primer reporte de un procedimiento en el seno frontal realizado por Wells quien curó a un paciente de un piocele frontal por medio de un drenaje externo e intranasal. Veinte años después, Schaeffer basado en disecciones anatómicas que vinculaban al drenaje del seno frontal con el infundíbulo en el meato medio anterior concluyó que un abordaje intranasal era posible para drenar los procesos supurativos crónicos sin un mayor riesgo que los abordajes externos. Se establece entonces el concepto que una adecuada función del conducto nasofrontal es indispensable para mantener ventilado y funcionante al seno frontal. Entre 1900 y 1910 diversos autores como Ingalls, Halle y Good avocaron los procedimientos intranasales para desobstruir el conducto nasofrontal. Sin embargo, estos reportes cayeron en popularidad debido a que se publicaron artículos que nombraban la morbilidad significativa e incluso mortalidad dada por la punción inadvertida de la cavidad craneal (12).
En 1884 Ogston publicó una detallada técnica para el abordaje externo al SF. Utilizó una incisión vertical en la línea media de la frente, levantó un colgajo subperiosteal y expuso la tabla anterior. Trepanó el seno del tamaño de una “six-penny piece” y se evacuó el material purulento. Luego dilató el conducto nasofrontal y colocó un tubo de drenaje entre el SF y la cavidad nasal. También reportó que cureteó la mucosa en la región del conducto nasofrontal. En 1896 Luc reporta una técnica similar en la literatura francesa (12).
Esta técnica de Ogston-Luc tuvo una alta tasa de fracaso atribuible al cierre de la comunicación frontonasal.
En 1895 Kuhnt, describión otro procedimiento externo en el cual extraía la totalidad de la tabla anterior, suprimió la mucosa de la porción superior del conducto nasofrontal y colocó un stent a través del conducto para mantener el drenaje temporariamente. La obliteración del seno se realizó con la piel anterior contra la tabla posterior.
Coakley resumió los abordajes vigentes en la época para el tratamiento de la supuración frontal de la siguiente manera. Primero realizar una vasoconstricción intranasal con cocaína. La porción anterior del cornete medio se extrae para dejar descubierto el conducto frontal seguida de la irrigación así como la dilatación del mismo para promover el drenaje. Cuando este abordaje fallaba en controlar la infección era necesario un abordaje externo (12).
Lack reportó que con estas intervenciones vía externa el éxito era ocasional y los pacientes desarrollaban una desfiguración cosmética significativa. Logan-Turner informaron que la operación de Ogston-Luc fracasaba en más del 50% de los casos. Riedel-Schenke introdujeron el primer procedimiento obliterativo radical completo en 1898. Se resecó el hueso de la tabla anterior y del piso, la mucosa del piso se resecó en su totalidad. la piel de la frente se colapsó contra la tabla posterior. Sin embargo, las tasas de curación con este procedimiento no justificaban la muy importante deformidad cosmética que resultaba (1,12,19).
En 1903 Killian introdujo un variación de la técnica de Riedel donde preservaba el anillo supraorbitario y eliminaba un cierto grado de deformidad estética. Mediante este abordaje se realizaba la exenteración del laberinto etmoidal. También se creaba un flap mucoso de la nariz que se rotaba hasta el conducto nasofrontal. Luego se colocaba un stent del seno a la cavidad nasal y también hacia la porción lateral de la incisión cutánea brindando drenaje externo (12).
Desafortunadamente la técnica de Killian tenía algunos inconvenientes: la obliteración de las porciones distales del SF a menudo eran incompletas , necrosis del anillo supraorbitario que llevaron a deformidades estéticas y varios casos se cerraba durante el postoperatorio el conducto nasofrontal.
En 1903 Hajek introdujo los primeros conceptos de una operación osteoplástica del SF. La deformidad cosmética podría ser eliminada creando un colgajo óseo de la pared anterior que se reponía en la misma posición luego de la inspección y la remoción de la mucosa enferma. El drenaje intranasal se facilitaba removiendo las celdillas etmoidales anteriores e insertando un tubo a traves de la cavidad quirúrgica y la nariz. La función del conducto nsaofrontal era necesaria para asegurar el éxito quirúrgico (12). Infección recurrente atribuible a la obstrucción secunadria del conducto nasofrontal era una secuela común luego de la extracción del tubo de drenaje 6 a 12 semanas luego del postoperatorio.
Desde 1915 a 1917 Lothrop introdujo un procedimiento donde creaba un comunicación nasofrontal amplia basado en que el cierre del conducto estaba dado por la estrechez del mismo. Lothrop creía que si se establecía el libre drenaje todos los síntomas subjetivos resolverían. Resecaba el complejo etmoidal anterior junto con el piso del seno frontal anterior, el septo interfrontal y la porción superior del septo nasal. Técnicamente dificultosa y dado que seguían ocurriendo las estenosis del conducto nasofrontal esta técnica no solía utilizarse (12).
En 1921 Lynch publica una serie de 15 casos con un seguimiento de 30 meses. Lynch realizaba la exenteración del laberinto etmoidal mediante una incisión periorbitaria medial, sugiriendo la remoción completa de la lámina papirácea y el proceso frontal de la maxila. También removía el piso del SF para acceder a curetear la mucosa del seno, colocaba un tubo de drenaje por 5 días y la comunicación nasofrontal era dilatada por 10 días durante el postoperatorio.
Más adelante surgieron reportes donde se hablaba de las infecciones recurrentes debidas aparentemente por el cierre del conducto nasofrontal (CNF). El tejido de granulación orbitario de la etmidectomía externa se adhería a la traumatizada mucosa del CNF creando tejido cicatrizal y estenosando el conducto (12).
Mientras ocurría esto informes esporádicos surgían utilizando una vía intranasal para drenar el seno. Mosher describió un abordaje en el que cureteaba el etmoides anterior y el agger nasi para abrir el CNF y proveer de drebaje al seno. En 1927 Lillie y Anderson sugirieron una operación en dos tiempos donde inicialmente se agrandaba el CNF mediante la resección del agger nasi y cureteando el ostium para ensanchar la comunicación. Si los síntomas persistían se realizaba una técnica de Killian o Lynch.
En 1935 Good publicó resultados de más de 300 procedimientos intranasales que incluían el raspado del labio anterior óseo del ostium frontal. Sugería que con esta técnica por lo menos aliviaba los síntomas de sus pacientes (12). En 1940 Williams y Mousel recomendaron el abordaje intranasal para la enfermedad frontoetmoidal si la anatomía permitía que esta técnica fuera segura. Además informaron que las técnicas intranasales requerían de mayor habilidad manual y eran técnicamente más delicadas, además de resultar más peligrosas que las técnicas externas (12).
En 1942 Goodale resumió las fallas en la técnica de Lynch. Al menos 30 pacientes de 106 operados requirieron una cirugía adicional. El principal fracaso era debido a la estenosis del CNF por tejido de cicatrización. Debido a que la mayoría de los fracasos de la técnica no obliterativa era el cierre secundario del CNF una gran variedad de métodos surgieron para lograr un CNF permeable. Incluyó el uso de tubos , stents, injertos y colgajos. Los tubos eran de diversos materiales como goma, acrílico, oro y dacron12.
Debido a que continuaron los informes relatando una tasa de fracaso del 30% con la frontoetmoidectomía de Lynch sumado a la visión dificultosa de las porciones distales de los grandes senos, la escuela osteoplástica fue ganando terreno. Esta técnica provee de una excelente visión dentro del seno. Este abordaje era ideal para el tratamiento de osteomas, celdillas frontoetmoidales obstruída, mucopioceles y enfermedad inflamatoria crónica irreversible. Incluso un problema localizado podía manejarse mediante una remoción parcial de la mucosa sin llegar a la obliteración del SF. Esta técnica provee de una visualización directa de uno o amnos senos y cuando se combina con la obliteración elimina la necesidad de dejar permeable el CNF (12).
La técnica osteoplástica fue practicada inicialmente por Brieger y Schornborn en 1894. En Latinoamérica la cirugía osteoplástica del SF fue popularizada y modificada por Bergara y Tato en 1953 (13). En Estados Unidos sus seguidores fueron Goodale y Montgomery en 1958. A pesar de la excelente visualización que provee esta técnica se asocia con una alta morbilidad y deformidad cosmética. Hardy y Montgomery informaron acerca de una incidencia del 19% de fístulas de líquido cefalorraquídeo, y de 208 pacientes 35% se quejaron de parestesia o anestesia frontal persistente y 20 requirieron cirugía de revisión. Cefaleas en 6% aún sin evidencia de enfermedad sinusal (12).
El desarrollo de los endoscopios cambió dramaticamente el manejo de la enfermedad sinusal. En 1879 Nitze inventó el citoscopio que en 1901 Hirschman introdujo dentro del seno maxilar. En esta época la visualización del seno servía solo como un instrumento de diagnóstico. En 1922 Spielberg publica un informe describiendo un antroscopio para poder examinar dentro del seno maxilar a través del meato inferior. En 1925 Maltz propone el término “sinoscopy” y Wolf en Berlín construye un improvisado instrumento óptico. Luego hubo poco desarrollo en estas ópticas hasta la llegada de las fibras ópticas. Le siguieron el desarrollo de ópticas anguladas de 30 y 70 grados incrementando de esta manera la visualización de las estructuras nasales y paranasales. En 1970 las técnicas endoscópicas se desparramaron por toda Europa. Messerklinger obtuvo fotos con gran detalle de la intrincada pared lateronasal que fueron combinadas con datos de la TC (12).
Abordajes externos al seno frontal
Introducción
Nuevas técnicas fueron evolucionando de la mano de una revolucionaria tecnología que apunta a la cirugía mínimanente invasiva como es la cirugía endoscópica nasal. Los procedimientos que se realizan actualmente mediante los endoscopios varían drásticamente a los que pudieran realizarse en 1985 debido al refinamiento de los tornos, debridadores, pinzas y a la reciente cirugía guiada por imágenes.
Cirugías como la obliteración del seno frontal, trepanación del SF y la fontoetmoidectomía externa están extensamente desarrolladas en la literatura con sus indicaciones, éxitos y tasas de complicaciones bien documentadas (10).
Es por ello que a continuación se desarrollará las actuales indicaciones de estas técnicas discutiendo su utilidad de manera individual en comparación con la técnica endoscópica.
Trepanación al seno frontal
Indicaciones
Es la cirugía por vía externa que probablemente presenta más utilidad en la era de los endoscopios (10). Son candidatos pacientes que presentan una sinusitis frontal aguda o una exacerbación aguda de una sinusitis crónica que no responde al tratamiento médico local y sistémico. Cuando existe la formación de un absceso subperióstico u osteomielitis referido como tumor de Pott (10). Cuando el paciente persiste con dolor persistente e inflamación del párpado superior después de 48hs de tratamiento, si hay progresión de la enfermedad o si existe una complicación orbitaria o intracraneana debe considerarse una trepanación (9). En otros casos puede realizarse una trepanación cuando se requiera un cultivo o una biopsia de una enfemedad del seno frontal.
Sin embargo, otros autores como Messerklinger, Stammberger y Wolf prefieren para estos casos un abordaje endoscópico al receso frontal aunque se requiere de experiencia para realizar dicho procedimiento (1). El abordaje endoscópico en el transcurso de una sinusitis frontal aguda resulta en intenso sangrado y mala visibilidad por una mucosa edematosa e inflamada. Las ventajas son que resulta en una menor morbilidad y soluciona el problema obstructivo en el mismo procedimiento. Actualmente cada vez más rinólogos van haciéndose adeptos a este procedimiento (1). Las desventajas son que puede requerirse de una cirugía guiada por imágenes (no disponible en todos los centros), mayor tiempo operatorio (la trepanación puede realizarse en 30 minutos) y la posibilidad de crear una sinequia por fibrosis del receso con posibilidad de revisión quirúrgica (10). La trepanación no deja una cicatriz de gran importancia estética.
Otra indicación de la trepanación es la identificación del SF en cirugía endoscópica de revisión (sinusitis crónica). Puede instilarse solución salina o instalar un pequeño cateter para identificar el tracto de drenaje del seno (10,11) (fig.10).
Técnica
Siempre debe realizarse habiendo obtenido previamente una imagen de los SF. Paciente en decúbito dorsal se traza una línea vertical mediana y una línea horizaontal que pasa por ambos agujeros supraorbitarios, luego la bisectriz en ángulo recto formado por las dos líneas precedentes en el lado del seno a trepanar (fig.11). El lugar de punción preconizado por Lermoyne está a 1cm del pie de la bisectriz (14).
Debe hacerse la incisión por encima del ligamento angular interno evitando lesionar el ojo. La trepanación se hace en el piso o cerca del mismo. No debe irrigarse si existe una dehiscencia del techo ya que puede ser causa de ceguera (11).
La trepanación puede realizarse con anestesia local o general. Infiltración con lidocaína con epinefrina. Incisión de 2cm de longitud curva por debajo del sector medial de la ceja (9) (fig. 12). Debe llegarse hasta el periostio exponiendo el hueso. Con una espátula o perióstomo se descubre el hueso justo por debajo de la eminencia del SF. Puede controlarse el punto de entrada mediante las radiografías. Mediante una fresa chica o con cureta se ingresa al seno (fig.13). Si existe material purulento recordar enviar para cultivo. Irrigar el seno con solución salina de manera suave. Evitar en lo posible sondear el ostium frontal porque puede dar lugar a estenosis. Puede introducirse a través de la trepanación un endoscopio para visualizar el seno, especialmente la pared posterior que debe estar intacta (11).
Si la intervención es debida a una sinusitis aguda puede dejarse dos tubos de plástico para drenaje y para instilaciones durante el postoperatorio(fig.14). Se debe advertir al paciente sobre la posible anestesia de la región del nervio supratroclear que es común y suele desaparecer con el tiempo. Se debe evitar el traumatismo sobre el nervio supraorbitario (9).
Frontoetmoidectomía externa (Lynch)
Indicaciones
Es una técnica que hoy día tiene escasa utilización (10). Puede utilizarse para el tratamiento de la sinusitis crónica (escasas ocasiones), remoción de osteomas y mucoceles, biopsia y excisión de tumores de la región (9). Para algunos autores es menos invasiva que la cirugía osteoplástica y permite el tratamiento del etmoides simultáneamente. Sin embargo, presenta tasas de fracaso que van del 20 al 30% (9). Por otro lado, dado que esta técnica consiste en una etmoidectomía más una resección del piso del SF acarrea la tendencia a formar cicatrices en el áerea del CNF. Es por ello que autores como Murr (10) prefieren utilizar esta técnica cuando no hay disponibilidad de instrumentos endoscópicos adecuados o cuando el cirujano no está seguro del abordaje transnasal endoscópico. Puede utilizarse esta técnica para procesos oncológicos. También puede considerarse esta técnica en aquellos casos donde exista una importante estenosis del receso frontal debido a reiteradas cirugías endoscópicas. Otras indicaciones para Loré (11) son fístula externa, complicaciones orbitarias menores, poliposis severas y papilomatosis invertida. Si no hubiera afección etmoidal puede considerarse a la cirugía osteoplástica como primera opción de abordaje externo. Las consideraciones sobresalientes según Lore para esta tecnica son (11): una hemostasia meticulosa, evitar lesionar el ojo y estructuras asociadas (ligamento palpebral interno, saco y conducto lacrimal), cuidado de perforar lámina cribosa, preservar tanta mucosa como sea posible, las dehiscencias óseas pueden acarrear la entrada a la fosa craneana anterior. Se debe eliminar todo el piso del SF y establecer una nueva y amplia comunicación nasofrontal que es uno de los objetivos principales de la operación. Debe eliminarse toda desviación alta del septo nasal con cuidado de no lesionar la lámina cribosa.
Técnica
Anestesia general. Infiltración de lidocaína con epinefrina. Incisión curvilínea de 2,5 a 3,5 cm de largo a 1cm por debajo del nivel del ligamento palpebral interno (fig.15). Se realiza una tarsorrafia temporaria para protección del globo ocular. Se expone los músculos orbicular de los párpados y porción superior del elevador propio del labio superior y también los vasos palpebrales superiores (ramas de los vasos angulares) que se ligan o electrocoagulan. Se expone y preserva el ligamento palpebral interno (9,11).
Se incide el periostio, se levanta y retrae lateralmente, liberando cuidadosamente la porción superior del saco lacrimal. Se expone toda la lámina papirácea y el piso del seno frontal. Se debe evitar el desgarro del periostio y de la fascia periorbitaria (especialmente en la sutura frontoetmoidal donde está bien adherida) para evitar la herniación de la grasa orbitaria. Se colocan separadores. Se ligan las arterias etmoidales anterior y posterior (fig.16) (11).
En un punto ubicado justo por detrás de la fosa lacrimal se penetra la pared orbitaria interna con un perforador aguda. Mediante pinza Kerrison y cureta se elimina el hueso situado posteriormente (fig.17 línea punteada), incluyendo el borde posterior del proceso nasal del maxilar superior (preservar mucosa nasal) y desde allí, el unguis y la lámina papirácea. Se eliminan las celdillas etmoidales anteriores. Se elimina de esta manera el hueso superointerno de la órbita penetrando al seno frontal y retirando todo el piso de este seno. Algunos autores en este punto advierten de la resección total de la mucosa que sería beneficioso evitando recidivas de sinusitis frontales o poliposis severas (11), para otros es indispensable preservar cuanta mucosa se pueda sobre toda la altura del CNF para evitar de esta manera la estenosis del mismo que conlleva al fracaso quirúrgico (9).
Se elimina todo lo que se pueda del cornete medio para permitir una comunicación adecuada con la cavidad nasal. Puede requerirse asimismo la eliminación de las celdillas etmoidales posteriores que se realiz ameidante pinzas gubias.
Si se extrajo toda la mucosa del SF puede utilizarse un colgajo mucoperióstico nasal para revestir la nueva comunicación nasofrontal. Se aplica un tubo intranasal de silastic que vaya hasta el seno y se deja entre 1 y 3 meses (fig.18) (11). Este tubo se sutura al piso de la cavidad nasal para impedir que se salga.
Las complicaciones descriptas para esta intervención son: hemorragia, lesiones orbitarias, estenosis del CNF y perforación de la lámina cribosa del etmoides o de la pared interna del SF, hacia la duramadre (11).
Abordaje Osteoplástico al seno frontal con o sin obliteración
Es un procedimiento que permite una visualización directa y binocular con alta tasa de éxito. Cuando se procede a obliterar el seno debe comprenderse que se elimina la función del mismo, lo inabilita (10,19). Muchas escuelas utilizan este abordajes teniendo un extenso seguimiento de los pacientes y lo recomiendan (16).
En algunos centros se compara este procedimiento con la técnica de Lothrop endoscópica. Esto lleva a controversias debido a que continua siendo un procedimiento poco utilizado y no está claro si realmente es una técnica funcional debido a que no parece preservar la función ciliar fisiológica (10).
Otra ventaja de esta técnica es que permite un abordaje directo a la tabla posterior y la duramadre. Entre las desventajas se encuentran que presenta una cierta morbilidad con no muy buena aceptación por parte del paciente hoy día. Potencial riesgo de infección de la herida y del sitio donante (extracción de grasa). La supuración del injerto de grasa es infrecuente. Un inadecuado cierre del periostio puede llevar a una depresión forntal (19).
Las recurrencias ocurren en un bajo porcentaje de casos y generalmente está asociada a una remoción incompleta de la mucosa. Es por ello que es esencial el fresado de la tabla interna erradicando todo vestigio de mucosa. Otra causa de fracaso es la inadecuada oclusión del CNF que puede hacerse con músculo, facia o hidroxiapatita. Por otro lado si persiste la patología en el receso frontal esta técnica fracasará es por ello que en algunos casos puede requerirse un abordaje combinado (1,19).
La extensa neumatización del SF también puede ser un problema para la adecuada obliteración. Además la neumatización de las celdillas supraorbitarias puede interferir con una buena visualización del seno (19).
Indicaciones
Rinosinusitis crónica y poliposis nasal que ha sido refractaria al tratamiento endoscópico (aún habiendo realizado una apertura amplia tipo II o III de Draf) y cuando el receso frontal se encuentra cicatrizado, osteítico o ambos (9,18). Puede utilizarse como primera opción el los casos de anatomía muy desfavorable como un RF muy estrecho o celdas frontales tipo IV. En los casos de complicaciones orbitarias o intracraneales debido a sinusitis frontal puede utilizarse esta vía (9). Es el procedimiento de elección para los osteomas sintomáticos (17) y para las disquinecias ciliares primarias y fibrosis quística. También es de elección para el tratamiento de las fracturas frontales ya sea de la tabla anterior o la posterior. Puede también tratarse mediante este abordaje tumores como el papiloma invertido donde se recomienda no obliterar el seno para poder realizar un correcto seguimiento pot imágenes o seudo tumores como la displasia fibrosa (9,10,18).
Las consideraciones que realiza Loré son:(11)
Una evaluación oftalmológica preoperatoria. Se debe usar un patrón radiográfico del seno frontal utilizando técnica de Caldwell. Es conveniente realizar una incisión cosmética por arriba o debajo de la ceja, también puede utilizarse una incisión coronal bajo la línea de los cabellos. Si la mucosa se encuentra enferma debe eliminarse de manera completa y meticulosa con una fresa, el CNF debe obliterarse. En estos casos la cavidad tendería a llenarse mediante osteoneogénesis y la formación de tejido cicatrizal. Es por ello que Bergara y Tato promueven la obliteración del seno utilizando grasa la cual se mantendría viable a lo largo del tiempo (13,18,19). Por el contrario, si la mucosa presenta aspecto normal como ocurre por ejemplo en un osteoma debe preservarse meticulosamente (17).
No deben afeitarse las cejas ya que podrían no regenerarse. Es opcional realizar una tarsorrafia durante el procedimiento. Si existe infección recordar tomar una muestra y enviar para cultivo y antibiograma.
Contraindicaciones
– Erosión de la tabla posterior.
– Erosión del techo orbitario.
– Celdillas etmoidales supraorbitarias hiperneumatizadas.
– Sinusitis fúngica alérgica (controvertido).
– Papiloma invertido (no para todos los autores (19)) o tumor maligno (recidivas).
Técnica
Se realiza una incisión por arriba (ligeramente curva) o por debajo de las cejas. En algunos casos puede requerirse una incisión bicoronal para acceder a ambos senos frontales (para algunos autores14 vía bicoronal de Unterberger). Con menos frecuencia puede usarse una incisión superciliar baja bilateral en “ala de mariposa” en pacientes calvos o con riesgo de calvicie (Fig.19). Independiente del tipo de incisión utilizada los autores aconsejan la infiltración con lidocaína con epinefrina. Se forma un colgajo de piel con base superior de todas las capas del tejido hasta el periostio. Debe tenese cuidado de preservar los nervios supraorbitario y supratroclear. Se deja el periostio adherido al hueso. Se coloca el recorte de la radiografía del seno a operar, tratar que el recorte sea un poco más pequeño y con una radiografía tipo Caldwell tomada a 6 pies de distancia Se coloca sobre el seno y se hace una imcisión a través del periostio en los bordes superior, lateral e interno (fig.20). El borde inferior quedará intacto y será la “bisagra” para la ventana ósea anterior además de ser la fuente de irrigación sanguínea del colgajo osteoperióstico (fig.21).
Mediante una sierra sagital plana Stryker, se hace un corte y se bisela ligeramente hacia abajo y adentro protegiendo de esta forma los bordes del seno, evitando penetrar a la fosa craneana anterior y además sostiene el colgajo óseo al reponerlo (fig.22). Si no se tiene sierra puede utilizarse una fresa pequeña comedora pero es escencial la dirección de la misma que debe ser siempre dirigida al centro del SF.
Mediante un osteótomo a lo largo de las líneas de corte, se levanta y fractura el colgajo osteoperióstico que queda adherido a su borde inferior (fig.23)
El colgajo osteoperióstico se retrae hacia abajo exponiendo el SF. Se extrae la patología. En el caso que la mucosa se encuentre enferma se procede a su eliminación de manera meticulosa e incluyendo el CNF donde se invierte la mucosa hacia la fosa nasal. Se nivelan los espolones óseos utilizando una fresa pulidora destruyendo todo tipo de repliegue mucoso especialmente las inavginaciones dadas por las venas de Breschet. Se oblitera el CNF con músculo, facia o hueso.
El SF se rellena con grasa abdominal en su totalidad (extraída preferentemente del cuadrante inferior izquierdo para que no se confunda con una cicatriz de apendicectomía). Para brindar mejor irrigación a este injerto puede fresarse la cortical interna de todo el seno (fig.24). El colgajo osteoperióstico se repone y se sutura con hilo reabsorbible 4-0 de manera cautelosa ya que un cierre defectuoso lleva a deformaciones estéticas ulteriores (fig.25). La piel se cierra en dos planos. Se deja drenaje cutáneo solo si existe infección activa.
En ciertas ocaciones puede abordarse el seno contralateral mediante esta exposición y eliminando el tabique intersinusal. En otros casos podrá utilizarse otros tipos de incisión descriptos al comienzo aunque la vía bicoronal puede asociarse a mayor pérdida sanguínea y la disección es más dificultosa
La complicaciones intraoperatorias se detallan en la Tabla II de acuerdo a un trabajo reciente realizado en 82 abordajes osteoplásticos de Weber y Draf (19).
Complicaciones postoperatorias:
Del seno frontal obliterado
– Traumatismo a la duramadre o al cerebro.
– Infeciones/osteomielitis.
– mucoceles.
– dolor crónico (nervio supraorbitario y supratroclear).
– Parestesia/Hipoestesia.
– Defectos óseos.
Del sitio donante
– Seroma
– Hematoma
– Celulitis o absceso
La TC no logra distinguir durante el postoperatorio entre fibrosis y sinusitis. Según el trabajo de Weber y Draf (18) los pacientes que presentan síntomas postoperatorios tardíos no tienen rasgos distintivos en la RMN al compararlo con los pacientes asintomáticos. Por otro lado, en dicho estudio concluyeron que los resultados clínicos parecen ser independientes de la viabilidad del injerto de grasa. Recomiendan esta técnica quirúrgica (en los casos que tienen indicación) reportando una tasa de éxito de 90% de éxito. Como complicaiones informaron acerca de un 9,8% de mucoceles y en estos casos la RMN es el método de elección.
El estudio a largo plazo de los senos obliterados con RMN revelan que la cantidad de grasa que sobrevive decrece con el tiempo, con la mayoría de los pacientes presentando menos de 20% de grasa remanente (la vida media es de 15,4meses)(18,35).
Abordaje Endoscópico al Seno Frontal
A medida que los cirujanos rinosinusales fueron ganando experiencia en cirugía endoscópica la idea de abordar al SF por esta vía y a través del receso frontal se hizo posible. Las ventajas son que se evita una cicatriz externa, se preserva el soporte de la pared lateral y se trata la patología etmoidal. Las desventajas son que es técnicamente difícil y existe el riesgo iatrogénico de estenosis del ostium frontal. Se debe estar seguro en las indicaciones precisas de la patología del SF y en muchos casos basta con la apertura del etmoides anterior y del agger nasi liberando de esta manera el drenaje del seno (19).
El éxito de la cirugía endoscópica frontal depende y requiere del conocimiento de la compleja anatomía local y de las variantes más comunes, análisis cuidadoso de la TC y una presisa disección de la anatomía del rededor. Los autores recomiendan observar con detenimiento las imágenes y principalmente el proceso uncinado y el agger nasi. Si el proceso uncinado se inserta en la pared lateral de la órbita (fig.7 A), lo que ocurre en 85% de los cadáveres, el receso frontal estará medial a la inserción de la unciforme. Si la unciforme se inserta en la fóvea o medial al cornete medio el receso estará lateral a la unciforme (fig.7 B y C). Muchas veces cuando está opacificado el seno es difícil de identificar la anatomía precisa de la unciforme (9).
Actualmente, se describen distintos abordajes y combinación de abordajes para tratar la patología frontal. Varios autores preconizan el tratamiento de una manera gradual, escalonada, donde la disección del receso frontal sería la primera opción a considerar (Tabla IV) (1,22). Tenerse en cuenta que la cirugía se basa en el dicho: “Do as little as possible, but as much as necessary” que significa realiza lo menos posible pero todo lo que sea necesario. Es por ello que la enfermedad leve requiere mínima cirugía y la enfermedad severa requerirá cirugía avanzada. Si el SF se encuantra libre en la TC y el paciente no sufre de cefalea frontal no es necesaria la exploración del receso frontal y mucho menos del SF.
fig26
Disección del receso frontal
En pacientes que presentan algún tipo de dolor o presión frontal y que también tienen un engrosamiento mucoso del SF en la TC el receso frontal debe explorarse. Un elemento clave es muchas veces la resección de una celdilla de agger nasi prominente. Puede también constatarse la permeabilidad del ostium a través de un aspirador curvo cuando exista un engrosamiento mucoso o simplemente visualizarlo con un endoscopio angulado para asegurarse de su permeablidad (22). La transiluminación endoscópica del SF intraoperatoria y postoperatoria es una manera simple y certera para ayudar a verificar la permeabilidad del seno (41).
Técnica
Se procede a realizar una etmoidectomía. Se reseca la parte superior de la unciforme. Apertura de celdilla agger nasi prominente con comedora de dirección para arriba (Hajek forceps, fig.26). El instrumento se coloca beneath la inserción anterior del cornete medio. Se extrae hueso de la parte superior y lateral para ensanchar la hendidura entre el cornete medio y la pared lateral dando de esta manera una visión directa del receso frontal. La remoción en este sitio se mantiene por delante de la cavidad craneal anterior. Por medio de curetas pueden extraerse remanentes de la celdilla etmoidal anterior de dirección posterior a anterior (fig.27). Luego puede introducirse una pinza tipo Blakesley dentro del receso para extraer fragmentos o mucosa enferma, se extrae solo tejido que sale facilmente. En este punto si el ostium todavía no ha sido visualizado puede pasarse de manera delicada un aspirador curvo o un explorador de ostium frontal de 1mm dentro del SF. El ostium está ubicado en una posición anterior y medial al receso frontal. Tener cuidado ya que puede haber celdillas supraorbitarias localizadas en un posición posterior y lateral al receso (22).
Stammberger (5) plantea lo que él denomina “Uncapping de Egg” para la apertura del receso. Si la unciforme, la bulla y las celdillas de agger nasi fueron resecadas y el ostium frontal no puede verse (para este autor es muy probable que esto ocurra) es porque queda una delgada cáscara ósea curvada remanente, que estaría en contacto con la base de cráneo o la lamella lateral del cornete medio. Esta delgada capa ósea bloquea el acceso al SF. Debe identificarse y removerse cautelosamente. Según este autor de esta manera raramente tendrá que realizarse una sinusotomía frontal drilando el nasal beak. Mediante curetas especiales curvadas o pinzas girafas se remueve la estructura descripta bajo buena visión y óptima hemostasia (fig.28). Debe ser una cirugía atraumática. Para esta maniobra se recomienda el uso de endoscopios angulados (30,45 o 70grados) y de punch cortantes circulares como el de la figura 29 (fig14 de fess stam).
La TC en sus cortes coronales y la endoscopía sirven para diagnosticar estos casos (fig.30). También Bradley y Kountakis concuerdan que el agger nasi muchas veces es la clave que hace fracasar la cirugía endoscópica del SF (24).
“Uncapping de egg” de Stamberger (5) fue descripto durante el tercer simposio internacional en FESS avanzado en 1995. Se explica de la siguiente manera: en un corte sagital la transición de SF a receso frontal tiene forma de reloj de arena, donde la cintura (estrictura) corresponde al ostium frontal. Este reloj puede asemejarse a un huevo colocado en un sostenedor de huevos (fig.31). Uno rompe el huevo y lo vacía, observa que la parte inferior del mismo (capa del huevo) permanece en el sostenedor. Si uno da vuelta esta situación puede asemejarse al receso frontal (fig.32). La parte vacía del sostenedor sería el infundíbulo del SF. La parte inferior con la cáscara del huevo sería el receso frontal (fig.33). El procedimiento consiste en remover esa cáscara del receso frontal (fig.34). Si uno tiene éxito las paredes del receso frontal no se traumatizarían y el pasaje del receso frontal al SF vía el ostium está libre. Según este autor, con este procedimiento sería muy raro tener que recurrir al fresado del nasal beak.
Idealmente, luego de este procedimiento las paredes del receso frontal deben estar cubiertas de mucosa. No debe traumatizarse de manera circular el ostium porque terminará en estenosis. Debe cuidarse de no fracturarse el cornete medio para prevenir la lateralización del mismo y de esta forma estenosando el receso frontal. La mucosa donde se inserta el cornete medio debe permanecer intacta. Si el cornete medio que desastibilizado puede crearse una sinequia del mismo con el septo como muestra la figura 35. Los stents y los drenajes no son de utilidad si la mucosa fue dañada o removida (5).
Sinusotomía Frontal Endoscópica
Aquellos pacientes que presentan patología avanzada en la TC (nivel hidroaéreo, opacificación) y síntomas relacionados a sinusitis frontal requiere el agrandamiento del ostium estenótico para aliviar los síntomas (22). Tiene la ventaja de eliminar el problema sin las morbilidades de los abordajes externos. Para ello se requiere de ópticas anguladas y de instrumental especial para SF1 (fig.36). También se han diseñado microdebridadores y drills especiales para traumatizar lo menos posible el receso frontal (25).
Si el ostium frontal no permite el pasaje de un explorador de 2mm o si se cree que está estenótico, puede abrirse en dirección anterior con una cureta, de esta manera se aleja de la cavidad craneal anterior. La cureta se coloca por arriba del receso frontal, encima del techo de la eminencia nasal, se rompe la pared posterior y superior de esta celdilla (fig. 37 y 38). El hueso grueso que se encuentra en posición anterior se conoce como frontal beak y dada la densidad del mismo puede requerirse del uso de drills o microdebridadores (fig.39). Se debe evitar el contacto con la región posterior del anillo del ostium frontal para evitar dañar la mucosa y por ende llevar a una cicatriz circunferencial e incluso osteoneogénesis (1,22). Metson no coloca rutinariamente stents o drenajes en la zona del ostium (22). Los restos óseos se extraen con pinzas girafas.
Los autores insisten en la conocimiento adecuado de la anatomía frontal y el cauteloso estudio preoperatorio de las TC (1,22). Actualmente, en algunos centros, esta cirugía se lleva a cabo asistida por un navegador de imágenes (1,27). Otros elementos a tener en cuenta en esta cirugía es una correcta hemostasia, siempre ejercer presión en sentido anterior (de posterior a anterior) y lateral (nunca medial), saber cuando cambiar a un procedimiento combinado y un cuidado meticuloso en el postoperatorio con una limpieza adecuada(1).
Abordaje por endoscopía y por trepanación
Se utiliza en aquellos casos donde se encuentra una celdilla frontal tipo III o IV (Tabla I) dentro del SF. En estos casos debe abrirse el receso por vía endoscópica. Si no logra detectarse las paredes de la celdilla frontal se realiza un trepanación de 4,5mm para obtener una mejor visualización y se procede a la resección de las paredes de dicha celdilla (fig.40)(1).
Lothrop intranasal modificada – Técnica de Draf
Draf desarrolló un estudio en 389 pacientes para describir esta técnica intranasal para restablecer el drenaje del SF. Dicho drenaje se obtiene resecando las celdillas etmoidales y el receso forntal junto con una parte medial de SF de acuerdo al proceso patológico. Es una de las vías más amplias de drenaje existiendo 3 estadíos (1) (Tabla V).
Sinusotomía Frontal Tipo Draf I (28,29)
Consiste en la remoción de la patología obstructiva inferior al ostium frontal. Se resecan las celdillas etmoidales anterosuperiores que obstruyen el receso frontal sin alterar el ostium frontal interno, lo expone.
En un estudio retrospectivo del autor (29) se evaluó 132 pacientes con un seguimiento postoperatorio de 5 años. Cuarenta y dos pacientes tenían una sinusotomía tipo I, 43 tipo II y 47 tipo III. El estudio endoscópico mostró una mucosa normal en 56-67%. No hubo recurrencias de complicaciones orbitarias o endocraneales. El éxito operatorio fue de 83,4% para el tipo I, 83,7% para el tipo II, 89,4% para el tipo III.
Este tipo de sinusotomía está indicada para restablecer el drenaje del SF cuando la historia clínica, el exámen físico y la TC sugiere que la sinusitis forntal crónica es consecuencia de la obstrucción del tracto de salida a nivel del receso frontal. Comienza con la movilización del cornete medio. Si el cornete se encuentra bulloso o polipoideo se realiza un turbinoplastia media. Se reseca totalmente el proceso uncinado. La bulla etmoidal puede preservarse o no dependiendo del caso. Si existen otros senos patológicos se tratarán y se deja para lo último el SF. Se resecan las celdillas anteriores del receso frontal. El ostium forntal se deja intacto.
Puede realizarse esta técnica utilizando microscopía con lentes de 250-300mm con espéculo autoestático o por medio de endoscopios angulados.
Sinusotomía Frontal Tipo Draf II(28)
Esta técnica consiste en agrandar el drenaje del SF o del CNF. Draf tipo IIA es la remoción de las celdillas etmoidales que protruyen dentro del SF, lo que fue descripto bajo el término “Uncapping the egg” descripto por Stamberger (5). Draf tipo IIB es la resección del piso del SF entre la lámina papirácea y el tabique nasal para proveer de una mayor apertura (fig.41). Este tipo de técnica se realiza si la historia, exámen físico y TC sugieren una sinusitis frontal complicada o como revisión de una sinusotomía tipo I fallida que presenta patología sinusal significativa como cicatrización amplia, pólipos y secreción viscosa. El procedimiento tipo II se recomienda para senos frontales con un diámetro antero-posterior amplio (anticipando un neo-ostium con un diámetro de 5mm o más), espina nasal interna hipoplásica y un extenso etmoides. En los casos de SF con un diámetro A-P pequeño, una espina nasal interna hiperplásica o un etmoides estrecho y en casos de revisión luego de haber realizado un drenaje tipo II, un tipo III se recomienda. También se recomienda utilizar el tipo III en poliposis severa o para remover osteomas, papilomas invertidos que involucra poco al SF y en casos seleccionados de fractura del SF limitados. Puede según este autor reducirse fracturas de la pared postero-inferior que involucre o no el techo etmoidal, incluso puede realizarse plásticas de duramadre endonasales en casos de un extenso diámetro A-P.
Para realizar estas técnicas resulta beneficioso el uso de navegación por imágenes. Además es importante considerar que la apertura más amplia que se realiza en la tipo IIB requiere el uso de tornos y punchs.
También el autor (28) aclara que en los casos de revisión puede ser necesaria la exposición del saco lagrimal para una orientación anatómica. En ambos tipos es esencial la conservación de toda la mucosa que sea posible.
Sinusotomía Frontal Tipo Draf III– Lothrop modificada (22,28,36,39)
Este tipo de procedimiento está indicado luego del fracaso de una previa sinusotomía tipo II o una cirugía de Lynch anterior, papilomas invertidos limitados y casos seleccionados de trauma. Se trata de un abordaje intranasal utilizando microscopio y torno para remover el piso del SF, el septo nasal superior y el septo interfrontal (fig.42). Close et al y Gross (31) describen un técnica similar pero utilizando endoscopios para crear una gran apertura. Se informó un tasa de éxito para esta técnica del 80% y parece ser más efectiva cuando se realiza de manera bilateral. Aunque la técnica obliterativa tiene un solo un 10% de fracasos (lothrop modificada 20%) algunos autores prefieren seguir utilizando la técnica tipo III debido a su baja morbilidad comparada con el abordaje externo.
Técnicamente es muy demandante debido a la estrecha anatomía del receso frontal, la angulación de los endoscopios y las secuelas de las cirugías previas. Se procede a la apertura de la pared anterior del receso frontal hasta identificar el ostium frontal. Se reseca la parte anterior y superior del ostium. En definitiva la técnica de Draf tipo IIB permite una apertura inicial del sector lateral del piso frontal. Se reseca 2 a 3 cm rectangular de septo nasal superior en la unión del cartílago cuadrangular y la porción perpendicular del etmoides, se reseca la parte medial del piso frontal (fig 43).
Luego de realizado esto, el triangulo de hueso formado por el piso frontal anterior (referido por May (32) como beak) en la línea media se remueve con fresado para obtener la máxima ventilación del seno. En casos especiales la identificación de la fibras olfatorias más anteriores sirven como límite posterior de la sinusotomía para evitar la perforación de la cribiforme.
Para algunos autores como Wormald (38) estas técnicas endoscópicas modificadas de Lothrop son una alternativa viable para la revisión de casos sintomáticos donde fue realizado una cirugía osteoplástica y presentan un mucocele en el seno frontal (40).
Los autores que describen estas técnicas utilizan taponaje por 3 a 7 días para hemostasia, humedecer la herida y para promover la reepitelización. Aquellos que utilizan stents lo dejan por 6 meses y reportan una alta tasa de éxito tras extensas cirugías endonasales (37) (fig.44). Sin embargo, el uso de stents como sus indicaciones continua siendo controversial.
Abordaje por endoscopía y por técnica osteoplástica
Se utiliza en los casos de patología similar a la combinación de endoscopía y trepanación pero cuando la trepanación no es suficiente para dicho tratamiento o la patología es muy grande y se necesita de una mayor incisión externa. Se remueve la patología por la técnica osteoplástica y se abre el receso vía endoscópica1.
Cranialización
La cranialización consiste en la remoción de la tabla posterior del seno frontal. Es un procedimiento que se desaconseja utilizar siendo muy precario y no respetando la fisiología rinosinusal. Omite por completo el receso frontal y, a largo plazo, lleva a las mismas complicaciones asociadas a la obliteración osteoplástica. El pericráneo remanente puede dar a la formación de un mucocele1.
Algunos autores (34) recomiendan este procedimiento para las fracturas múltiples del SF o para fracturas que involucran ambas tablas.
Cuidados Postoperatorios ( 22,28)
Este punto es de especial importancia en este tipo de cirugía para obtener éxito en los resultados. Los objetivos del postoperatorio son promover la curación de la mucosa y mantener la permeabilidad del ostium previniendo la cicatrización.
Algunos autores indican utilizar antibióticos por una semana. Otros lo utilizan si existe sinusitis aguda. Luego de la extracción del taponaje el paciente comienza con irrigaciones de solución salina nasales. Ëstas permiten la humidificación nasal y la limpieza atraumática. Restos y costras que obstruyan el drenaje o impidan la ventilación nasal se extraen durante la primer semana bajo visión endoscópica cuidando de no dañar el tejido de regeneración. Lo ideal es que la nariz no debería sangrar luego de la curación. Debe limpiarse de secreciones el área del receso frontal. Cualquier tipo de adhesión temprana deberá ser dividida con una cánula o pinza. Aquellos pacientes que presentan exposición del hueso durante el postoperatorio las limpiezas se prolongarán por más tiempo.
Los pacientes pueden aplicarse corticoides tópicos para reducir el edema postoperatorio y acelerar el proceso de curación. Pueden usarse hasta que la mucosa esté sana, por 6 meses o incluso en algunos casos por años. El uso de corticoide sistémico queda para pacientes con poliposis nasal recurrente, asma e intolerancia a la aspirina.
Navegación por imágenes en la cirugía del seno frontal
A mediados de los años 90´ comenzó la aplicación de la navegación por imágenes en la cirugía sinusal. Esta tecnología provee de una ubicación anatómica durante la cirugía brindando mayor seguridad y eficacia principalmente en cirugías complejas e intrincadas como lo es la cirugía del seno frontal (22). Los espacios estrechos del receso frontal y la proximidad de la órbita y la base de cráneo demandan alto grado de precisión técnica dejando poco margen de error (fig.45 y 46). Este tipo de tecnología ofrece la posibilidad de disminuir las complicaciones intraoperatorias y mejorar los resultados clínicos. El margen de error descripto actualmente va de 2mm al comienzo de la cirugía llegando a 1mm al finalizar el procedimiento (27). Además, estos sistemas pueden utilizarse tanto para cirugái endoscópica como para abordajes externos al SF mejorando la tasa de complicaciones incluso de estos últimos (33).
Hoy día los cirujanos rinosinusales concuerdan que este dispositivo resulta extremadamente beneficioso en los casos avanzados y en cirugía de revisión del SF, tanto para el planeamiento preoperatorio como para la localización intraoperatoria de la compleja anatomía de drenaje del SF. Por último Sindwani aclara que el uso de esta tecnología NO sustituye en absoluto un adecuado entrenamiento quirurgico y un conocimiento minucioso de la antomía rinosinusal (27).
Conclusiones
No cabe duda que los adelantos tecnológicos que trajeron el uso de la endoscopía en los campos operatorio han revolucionado la cirugía. La tendencia actual a la cirugía mínimamente invasiva es un hecho y el tratamiento de los senos paranasales entra dentro de este grupo.
El abordaje al seno frontal requiere un arduo entrenamiento en cirugía endoscópica con un certero conocimiento de la anatomía endonasal y sus variantes anatómicas. La selección de la técnica a emplear de acuerdo a la patología del paciente y los estudios preoperatorios de imágenes deben ser los primeros pasos para un resultado exitoso. Como dice el dicho enunciado anteriormente debe hacerse lo menos posible pero todo lo necesario para curar de enfermedad al seno frontal.
Actualmente siguen vigentes algunos abordajes externos al seno como ser la trepanación o la técnica osteoplástica. Dichas técnicas tienen indicaciones precisas y cada vez son utilizadas en menor medida. Sin embargo, el cirujano rinosinusal debe estar capacitado para acceder a estos abordajes cuando sea necesario, incluso en medio de una cirugía endoscópica (abordajes combinados).
En centros de alta complejidad de los países desarrollados se está empleando la navegación por imágenes. Dicho avance tecnológico es considerada un herramienta muy útil para este tipo de cirugía pero es solo una herramienta más y no debe reemplazar el conocimiento anatómico de los cirujano dedicados a este apasionante tema.
Anexo I – TABLAS
Tabla I. Clasificación de Bent y Kuhn para las celdillas frontales.
| Tipo I | Celdilla frontoetmoidal solitaria arriba de la celda de agger nasi, pero debajo del SF. |
| Tipo II | Fila de celdillas etmoideofrontales en el receso frontal arriba de la celda de agger nasi, pero debajo del SF. |
| Tipo III | Celdilla única grande que invade el seno frontal. |
| Tipo IV | Celdilla frontal aislada dentro del seno frontal. |
Modificado de : Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302 y de Cummings, C. Primary Sinus Surgery. Chapter: 61. En: Otolaryngology Head and Neck Surgery. Vol 2. 3ed. 1998. p:1145-1172.
Tabla II. Complicaciones Intraoperatorias en cirugía osteoplástica
|
Complicación
|
Número (%)
|
| Lesión de la periórbita | 16 (19,5%) |
| Ceguera | 0 |
| Fractura no intencional de la pared anterior del SF | 16 (19,5%) |
| Colgajo ósea muy pequeño | 7 (8,5%) |
| Colgajo óseo muy grande con exposición de duramadre | 5 (6%) |
| Lesión de duramadre | 8 (9,8%) |
Modificado de Weber, R. Draf, W. Osteoplastic Frontal Sinus Surgery Surgery With Fat Obliteration: Technique and Long-Term Results Using Magnetic Resonance Imaging in 82 Operations. Laryngoscope 2000;110:1037-1044.
Tabla III. Comparación de los abordajes externos al SF.
| Abordaje | Paredes Resecadas | Comentario |
| Reidel (1898) | Remoción completa de la pared anterior del SF | Deformación frente. Bueno para pequeños SF cuando sea imposible crear un colgajo osteoperióstico y en casos de osteomielitis de la tabla anterior. |
| Killian (1903) | Piso SF y pared anterior (preservación ridge supraorbitario); etmoidectomía | Deformidad de la frente, reconstrucción más sencilla que la de Reidel pero lo mismos problemas que Lynch |
| Lynch (1921) | Piso SF, parte de lámina papirácea, etmoidectomía | Al remover la pared lateral la órbita se prolapsa medialmente. No provee un acceso fácil al ostium natural. |
| Osteoplástica (Bergara-Tato) 1953 | No hay resección de paredes sino que rebate colgajo osteoperióstico anterior | Excelente exposición. Puede requerir extensas incisiones. Con o sin obliteración dependiendo la patología. Con obliteración difícil seguimiento mediante imágenes. |
Modificado de: Cummings: Otolaryngology: Head and Neck Surgery, 4th ed. 2005. p:1268-1273.
Tabla IV. Procedimientos actuales sobre el SF ordenados de una manera gradual.
| Disección del receso frontal |
| Sinusotomía Frontal Endoscópica |
| Endoscopía + Trepanación |
| Lothrop Intranasal modificado (Draf) |
| Endoscopía + Osteoplástica |
| Obliteración con Técnica Osteoplástica |
Modificado de: Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302 y Metson, R. Endoscopic surgery for frontal sinusitis- a graduated approach. Otolaryngol Clin N Am. 2004;37:411-422.
Tabla V. Drenaje endonasal del Seno Frontal según Draf y según May y Schaitkin28
| Clasificación Draf | Abordaje CNF May | Cirugía |
| I | I | Etmoidectomía anterior con drenaje del SF sin tocar el tracto de salida del seno. |
| II A | II | Remoción de las celdillas etmoidales que protruyen dentro del SF (“uncapping the egg”) creando una abertura entre el cornete medio medialmente y la lámina papirácea lateralmente. |
| B | III | Remoción del piso del SF entre el septo nasal medialmente y la lámina papirácea lateralmente (fig. 41). |
| III | IV | Drenaje tipo II en ambos lados y extracción de la parte superior del tabique nasal y la porción baja del septo del SF (fig.42). |
Extraído de: Weber, R. Draf, W. Modern Concepts in Frontal Sinus Surgery. Laryngoscope 2001 Volume 111(1):137-146.
Anexo II – FIGURAS
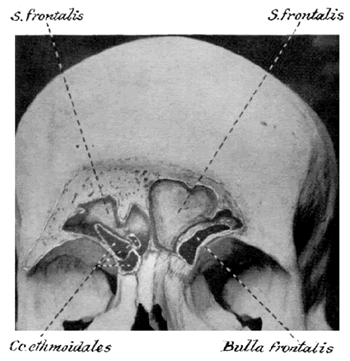
Fig1. Figura que muestra la antomía de los senos frontales.
Extraído de Jacobs, J. 100 years of Frontal Sinus Surgery. Laryngoscope 1997;suppl 107(11):1-36.
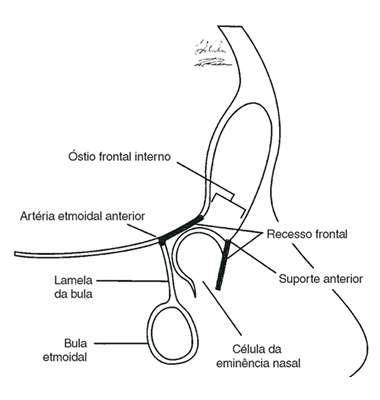
Fig.1 Esquema que muestra el receso frontal y las estructuras adyancentes.
Extraído de Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302.
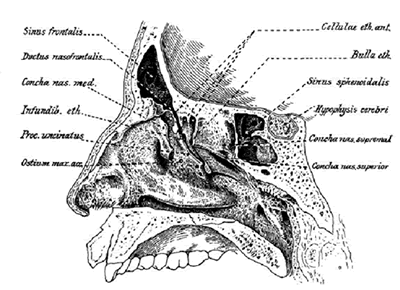
Fig2. Vista interna de la pared lateral de la cavidad nasal. Se observa el seno frontal, el conducto nasofrontal y la relación con el infundíbulo etmoidal y la apófisis unciforme.
Extraído de Jacobs, J. 100 years of Frontal Sinus Surgery. Laryngoscope 1997;suppl 107(11):1-36.
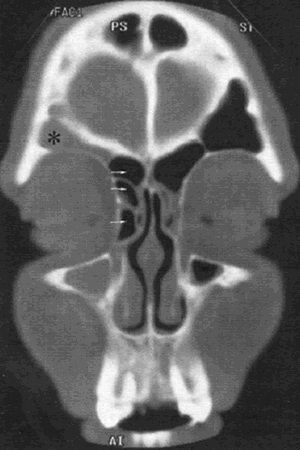
Fig.3 Corte coronal de TC que muestra celdilla de agger nasi y celdillas etmoidales anteriores (flechas)
asociada a una sinusitis frontal (asterisco).
Extraído de Jacobs, J. 100 years of Frontal Sinus Surgery. Laryngoscope1997;suppl 107(11):1-36.
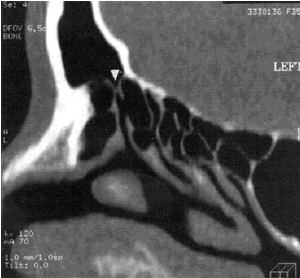
Fig.4 TC corte sagital. Se observa la obstrucción del receso frontal a expen sas de las celdillas etmoidales y del agger nasi.
En: Jacobs, J. 100 years of Frontal Sinus Surgery. Laryngoscope 1997;suppl 107(11):1-36.
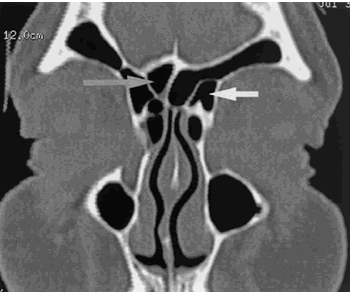
Fig.5 TC que muestra celdilla etmoideofrontal en el lado izquierdo empujando el seno frontal lateralmente y estrechando el ostim frontal (K3). Una celdilla etmoideofrontal medial (flecha gris) a la derecha empuja al seno medialmente (celdilla septal intersinusal, K3). Ver Tabla I. Clasificación de Khun.
En: Wormald, PJ. The agger nasi cell: The key to understanding the anatomy of
the frontal recess. Otolaryngology-Head and Neck Surgery 2003;129(5):497-507.
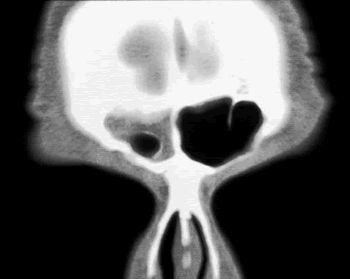
Fig.6. Celdilla frontal tipo IV de Khun. En: Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302.
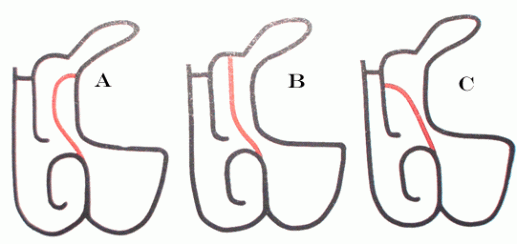
Fig.7 Variantes anatómicas de la inserción de la apófisis unciforme. A: a la pared lateral. B: a la lámina cribosa. C: al cornete medio. En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.

Fig.8 En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.
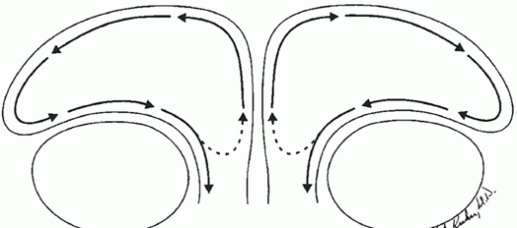
Fig.9 Esquema que muestra la circulación fisiológica del moco en el SF. En: Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302.
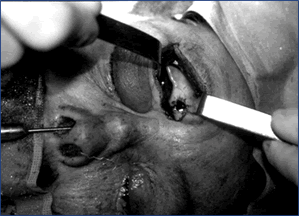
Fig.10 Trepanación del SF e identificación del ostium frontal vía endonasal
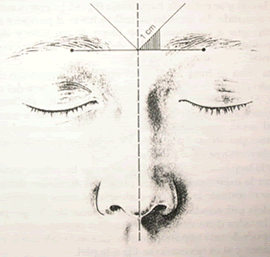
Fig.11 Zona de perforación en la trepanación del SF.
En: Enciclopedie Cirugía ORL. cirugía del seno frontal para lesiones no traumáticas ni tumorales. E-46-160
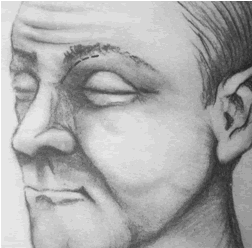
Fig.12 Incisión supraorbitaria. Extraído de: Loré. Los senos y el maxilar superior.
En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
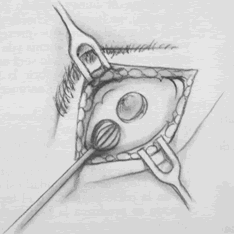
Fig.13. Fresado tabla anterior. Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.

Fig.14 Catéter para drenaje externo. Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
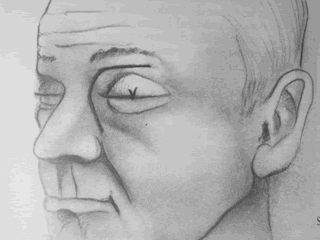
Fig. 15 Incisión de Lynch. Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
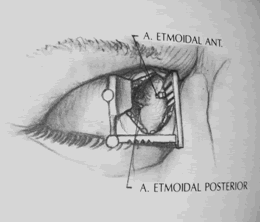
Fig.16 Ligadura de arteria etmoidal anterior y posterior.
Extraído de: Loré. Los senos y el maxilar superior.
En: Cirugía de cabeza y cuello. cap 5. Panamericana.
3 ed. 1990. p: 134-179.
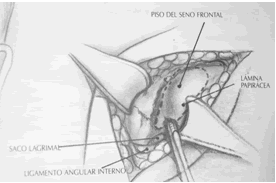
Fig. 17 Se elimina el hueso delimitado por la línea punteada.
Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.

Fig.18 Colocación tubo intranasal.
Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
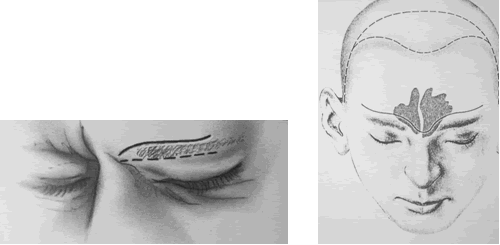
Fig.19 Incisiones que pueden realizarse en el abordaje osteoplástico. Superciliar, bicoronal y en ala de mariposa. Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179 y de Enciclopedie Cirugía ORL. cirugía del seno frontal para lesiones no traumáticas ni tumorales. E-46-160
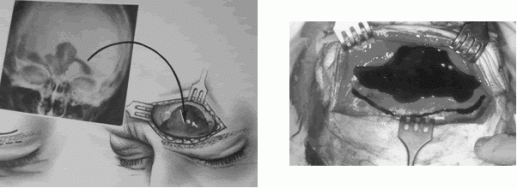
Fig.20 Marcado del seno frontal mediante placa radiográfica.
Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179 y de Weber, R. Draf, W. Osteoplastic Frontal Sinus Surgery Surgery With Fat Obliteration: Technique and Long-Term Results Using Magnetic Resonance Imaging in 82 Operations. Laryngoscope 2000;110:1037-1044.
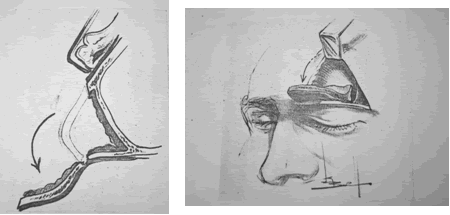
Fig. 21 El borde inferior queda intacto sirviendo como “bisagra” de la tabla anterior.
En: Tato, JM. Surgical Treatment of The Frontal Sinus by the External Route.
Laryngoscope 1954;64:504-21.
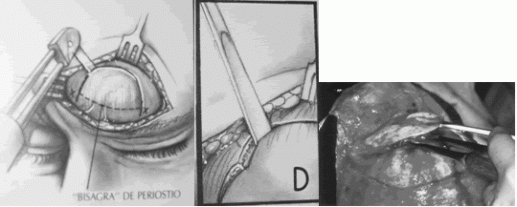
Fig. 22 y 23 Utilización de sierra Stryker para apertura de tabla anterior junto con osteótomo.
Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
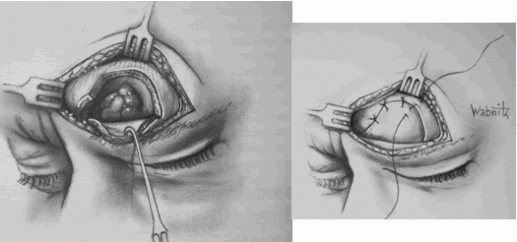
Fig. 24 Obliteración con grasa abdominal. Fig. 25 Cierre meticuloso del periostio.
Extraído de: Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.

Fig.26 Disección del receso frontal. Fosa nasal derecha. Apertura del agger nasi para agrandar la entrada al receso frontal. En: Metson, R. Endoscopic treatment of frontal sinusitis. Laryngoscope 1992;102:712-6.
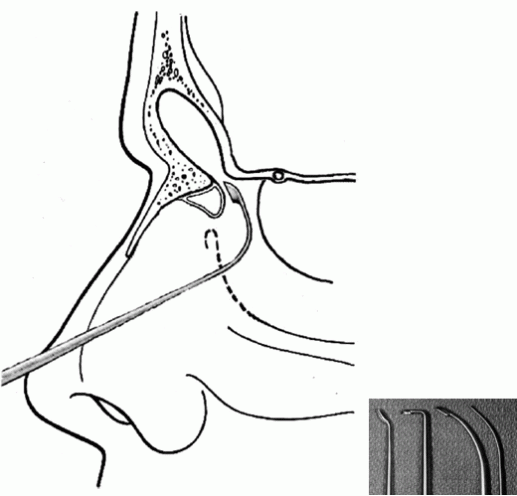
Fig.27 Esquema que muestra cureta durante una disección del receso frontal, debe dirigirse siguiendo una dirección posterior a anterior. Extraído de : Metson, R. Endoscopic surgery for frontal sinusitis- a graduated approach. Otolaryngol Clin N Am. 2004;37:411-422.
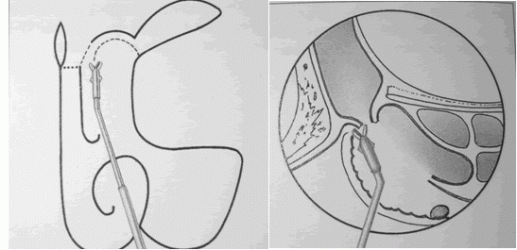
Fig. 28 Extracción de la delagada cobertura ósea “cap of the egg” con pinzas girafas.
En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.
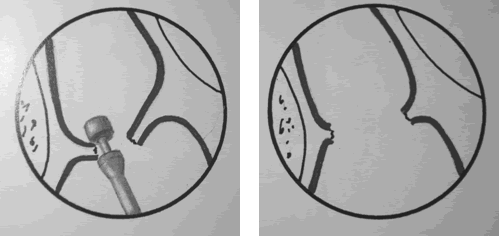
Fig.29 En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS
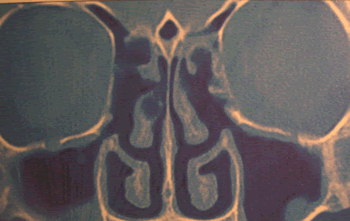
Fig.30 TC corte coronal. Hallazgo postoperatorio. A la izquierda del paciente una capa ósea de una celdilla de agger nasi no fue resecada resultando en una sinusitis frontal recurrente. En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.

En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.

Fig. 34 Resección del remanente de la “capa del huevo” del receso frontal para alcanzar el ostium frontal.
En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.
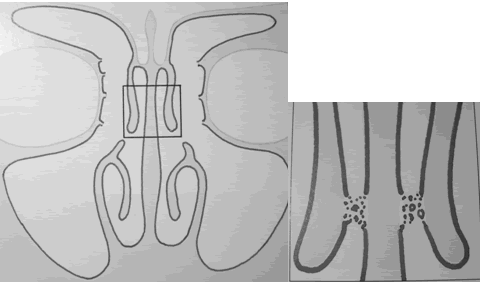
Fig. 35 Estabilización del cornete medio mediante la escarificación de dos pequeños sitios opuestos para que puedan adherirse. En: Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.
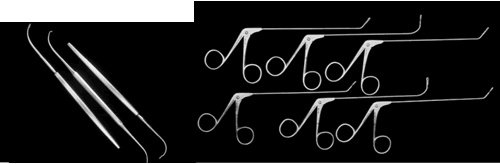
Fig. 36 Instrumental para cirugía endoscópica de SF. Exploradores y pinzas girafas.
En: Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302.
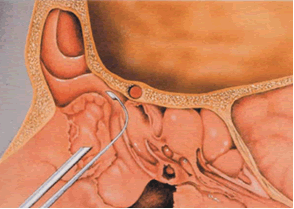
Fig. 37 Con una curtea de 90grados sobre el techo de la eminencia nasal se rompe las paredes posterior
y superior.
En: Kennedy, D. Cap 22. Cirurgia do Seio Frontal.
En: Doencas dos Seios Paranasais. Sao Paulo.
Ed: Revinter, 2004. p:281-302.
Fig.38 Sinusotomía frontal con cureta.
En: Metson, R.Endoscopic treatment of frontal sinusitis.Laryngoscope1992;102:712-6.
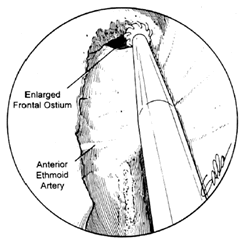
Fig.39 Sinusotomía frontal utilizando drill para agrandar ostium frontal. Extraído de: Metson, R.
Clinical outcome of endoscopic surgery for frontal sinusitis. Arch Otolaryngol Head Neck Surg 1998;124:1090-96.
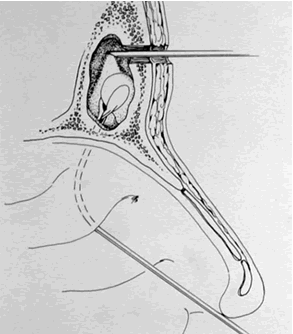
Fig.40 Abordaje combinado (trepanación y endoscopía).
En: Kennedy, D. Cap 22. Cirurgia do Seio Frontal.
En: Doencas dos Seios Paranasais. Sao Paulo.
Ed: Revinter, 2004. p:281-302.
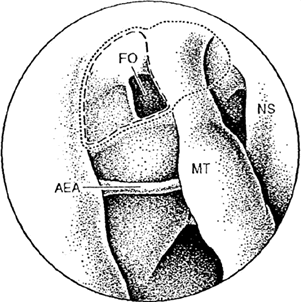
Fig.41 Vista endoscópica con resección con técnica de Draf IIB. Línea punteada. FO: ostium frontal. NS: septo nasal. AEA: Arteria etmoidal anterior. MT: cornete medio.
En: Weber, R. Draf, W. Modern Concepts in Frontal Sinus Surgery.
Laryngoscope 2001 Volume 111(1):137-146.
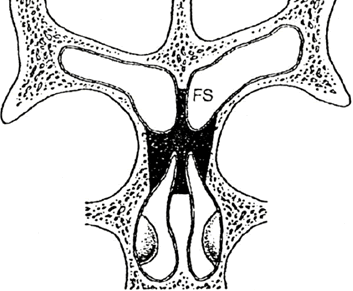
Fig.42 Vista coronal esquemática. Técnica de Draf III. Sombreado: áreas a resecar. FS: seno frontal.
En: Weber, R. Draf, W. Modern Concepts in Frontal Sinus Surgery.
Laryngoscope 2001 Volume 111(1):137-146.
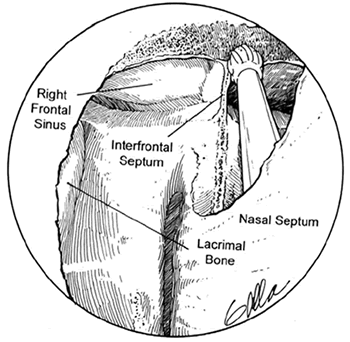
Fig. 43 Draf tipo III. Resección de la parte alta del septo nasal permitiendo la visualización para el drilado contralateral. También se reseca septo interfrontal y se abre el seno frontal contralateral.
En: Metson, R. Clinical outcome of endoscopic surgery for frontal sinusitis. Arch Otolaryngol Head Neck Surg 1998;124:1090-96.
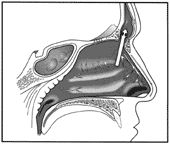
Fig.44 Rains Frontal Sinus Stent®. En: technique for insertion of rains frontal sinus stent by b. manrin rains iii, m.d., f.a.c.s
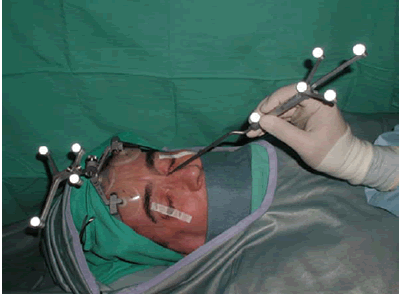
Fig.45 Set craneal y explorador de un sistema de navegación por imágenes basado en óptica (infrarojo) de Medtronic Xomed®. En: Sindwani, R. Image-Guided Frontal Sinus Surgery. Otolaryngol Clin N Am 2005;38:461-471.
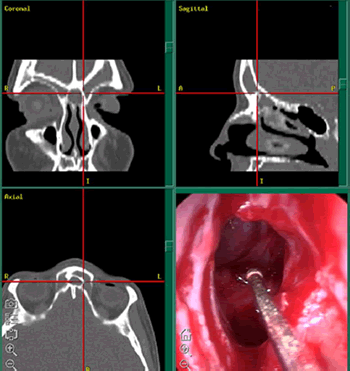
Fig.46 Vista intraoperatoria de una sinusotomía endoscópica guiada por imágenes tipo III de Draf.
En: Sindwani, R. Image-Guided Frontal Sinus Surgery. Otolaryngol Clin N Am 2005;38:461-471.
Referencias bibliográficas
1) Kennedy, D. Cap 22. Cirurgia do Seio Frontal. En: Doencas dos Seios Paranasais. Sao Paulo. Ed: Revinter, 2004. p:281-302.
2) Hassan Ramadan. History of Frontal Sinus Surgery. Arch Otolaryngol Head Neck Surg 2000; 126: 98-99.
3) Van Cauwenberge, P. Anatomy and physiology of the nose and the paranasal sinuses. Immunol Allergy Clin N Am. 2004;24:1-17.
4) Rouvière, H. Anatomía Humana. Tomo I. 9na ed. Masson. 1994. Pag 340-1
5) Stammberger, H. Uncapping the egg. The endoscopic approach to frontal recess and sinuses. FESS.
6)Stammberger HR, Kennedy DW. Paranasal sinuses: Anatomic terminology and nomenclature. The Anatomic Terminology Group. Ann Otol Rhinol Laryngol (Supl) 1995;167:7-16.
7) Wormald, PJ. The agger nasi cell: The key to understanding the anatomy of the frontal recess. Otolaryngology-Head and Neck Surgery 2003;129(5):497-507.
8) Sprekelsen, M. Bases anatómicas de las fosas nasales y de los senos paranasales. En: Cirugía Endoscópica Nasosinusal. Cap 1. 2da ed. 2001.
9) Cummings, C. Primary Sinus Surgery. Chapter: 61. En: Otolaryngology Head and Neck Surgery. Vol 2. 3ed. 1998. p:1145-1172.
10)Murr, A. Contemporary indications for external approaches to the paranasal sinuses. Otolaryngol Clin N Am 2004;37:423-434.
11)Loré. Los senos y el maxilar superior. En: Cirugía de cabeza y cuello. cap 5. Panamericana. 3 ed. 1990. p: 134-179.
12) Jacobs, J. 100 years of Frontal Sinus Surgery. Laryngoscope 1997;suppl 107(11):1-36.
13) Tato, JM. Surgical Treatment of The Frontal Sinus by the External Route. Laryngoscope 1954;64:504-21.
14) Enciclopedie Cirugía ORL. cirugía del seno frontal para lesiones no traumáticas ni tumorales. E-46-160
15) Kew, J. Multiplanar Reconstructed Computer Tomography Images Improves Depiction and Understanding of the Anatomy of Frontal Sinus and Recess. Am J Rhinol 2002;16(2):119-123.
16) Hardy, JM. Osteoplastic frontal sinusotomy: an analysis of 250 operations. Ann Otol Rhinol Laryngol 1976;85(4 part 1):523-32.
17) Lisete Pessoa de Oliveira Fobe. Cirurgia de osteoma de Seio Frontal. Arq Neuropsiquiatr 2002;60(1):101-105.
18) Weber, R. Draf, W. Osteoplastic Frontal Sinus Surgery Surgery With Fat Obliteration: Technique and Long-Term Results Using Magnetic Resonance Imaging in 82 Operations. Laryngoscope 2000;110:1037-1044.
19) Seiden, A. Frontal Sinus Surgery: The State of the Art. American Journal of Otolaryngology 1998;19(3):183-193.
20) Sousa, A. Importancia quirúrgica de la celdilla etmoidal del agger nasi. En: Revisión de temas.
21) Cummings: Otolaryngology: Head and Neck Surgery, 4th ed. 2005. p:1268-1273.
22) Metson, R. Endoscopic surgery for frontal sinusitis- a graduated approach. Otolaryngol Clin N Am. 2004;37:411-422.
23) Metson, R. Endoscopic treatment of frontal sinusitis. Laryngoscope 1992;102:712-6.
24) Bradley, D. The role of agger nasi air cells in patients requiring revision endoscopic frontal sinus surgery. Otolaryngol Head Neck Surg 2004;131:525-7.
25) Blokmanis, A. A new drill for frontal sinus surgery. Laryngoscope 2000;110:168-170.
26) Metson, R. Clinical outcome of endoscopic surgery for frontal sinusitis. Arch Otolaryngol Head Neck Surg 1998;124:1090-96.
27) Sindwani, R. Image-Guided Frontal Sinus Surgery. Otolaryngol Clin N Am 2005;38:461-471.
28) Weber, R. Draf, W. Modern Concepts in Frontal Sinus Surgery. Laryngoscope 2001 Volume 111(1):137-146.
29) Draf, W. Current aspects of frontal sinus surgery. I: Endonasal frontal sinus drainage in inflammatory diseases of the paranasal sinuses. HNO 1995 Jun;43(6):352-7. [abstract].
30) Weber, R. Current aspects of frontal sinus surgery. II: External frontal sinus operation–osteoplastic approach. HNO 1995 Jun;43(6):358-63. [abstract].
31) Close, L. Endoscopic resection of the intranasal frontal sinus floor. Ann Otol Rhinol Laryngol 1994;103:952-8.
32) May M, Schaitkin B. Frontal sinus surgery: endonasal drainage instead of an external osteoplastic approach. Operative Techniques in Otolaryngology—Head and Neck Surgery 1995; 6: 184–192.
33) Sindwani, R. Impact of image guidance on complications during osteoplastic frontal sinus surgery. Otolaryngol Head Neck Surg 2004;131:150-5.
34) Constantinidis, J. Cranialization of the frontal sinus. Indications, technique and results HNO 2000 May;48(5):361-6. [abstract]
35) Weber, R. Magnetic resonance imaging following fat obliteration of the frontal sinus. Neuroradiology2002Jan;44(1):52-8.
36) Sonnenburg, R. Revision Endoscopic Frontal Sinus Surgery. Curr Opin Otolaryngol Head Neck Surg 2004;12:49-52.
37) Weber, R. The success of 6-month stenting in endonasal frontal sinus surgery. ENT Journal 2000;79(12):930-941.
38) Wormald, P. Modified Endoscopic Lothrop as a Salvage for the Failed Osteoplastic Flap with Obliteration. Laryngoscope 2003;113:1988-1992.
39) Kikawada, T. Extended Endoscopic Frontal Sinus Surgery to Interrupted Nasofrontal Communication Caused by Scarring of the Anterior Ethmoid. Arch Otolaryngol Head Neck Surg 1999;125:92-96.
40) Langton-Hewer, C. Endoscopic sinus surgery rescue of failed osteoplastic flap with fat obliteration. Curr Opin Otolaryngol Head Neck Surg 2005;13:45-49.
41) Friedman, M. Frontal sinus surgery: Endoscopic Technique and Preliminary Results. Am J Rhinol 2000;14:393-403.

