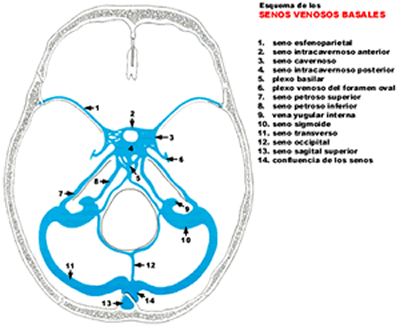
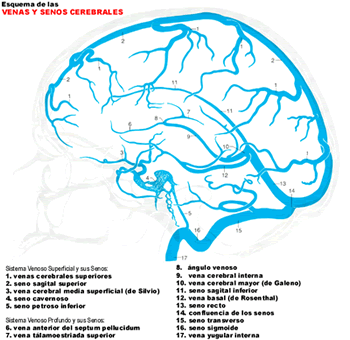
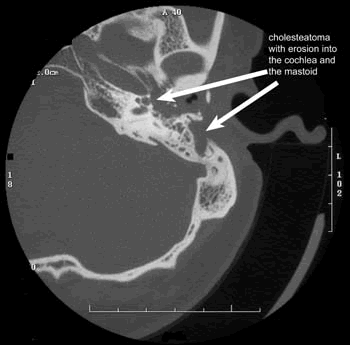
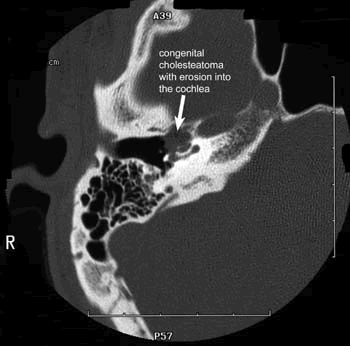
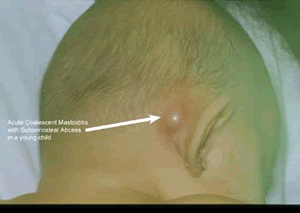
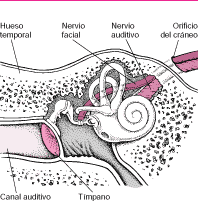
COMPLICACIONES INTRATEMPORALES DE LAS OTITIS
Complicaciones Intratemporales de las Otitis – Mortola Ana Florencia – 2006
Para poder visualizar el material completo y recibir mayor información, les solicitamos se registre aqui. Tenga en cuenta que de hacerlo nos sera de suma utilidad para seguir creciendo y difundiendo la especialidad.
INTRODUCCIÓN.
Las complicaciones de las otitis, tanto agudas como crónicas, han disminuido de manera importante tanto en su morbilidad como en su mortalidad, con la introducción de los quimioterápicos y antibióticos, pero no han desaparecido. Su aspecto ha cambiado y hoy es raro observar las clásicas mastoiditis agudas con sus grandes abscesos que eran la panacea de la ORL de antaño, ahora bien, si ya no se observan estas formas agudas, las formas subagudas siguen apareciendo, tratándose de procesos graves aunque con un pronóstico menos severo. Se ha de tener en cuenta que actualmente estas complicaciones están producidas muchas veces por bacterias resistentes a los antibióticos convencionales. La influencia del tratamiento antibioterápico, en numerosas ocasiones hace que su clínica esté modificada pudiendo dar lugar a cuadros raros o excepcionales. El diagnostico ha mejorado igualmente de forma notable gracias a las avanzadas técnicas de imagen de las que se disponen hoy día. Antiguamente estas complicaciones eran debidas sobre todo a la OMA virulenta, sin embargo en la actualidad se calcula que solo el 5% de estas complicaciones son debidas a OMA, o casos de reagudización de la misma, el resto de los casos se asocian a OMC y en especial al colesteatoma.
El descenso en la incidencia de estas complicaciones es debido a:
– El uso de agentes antimicrobianos.
– La mejor preparación el ORL para tratarlas y la mejora de las posibilidades quirúrgicas.
– El diagnostico más precoz y la mayor facilidad de acceso al especialista.
– La mejoría en general de los cuidados sanitarios de la población.
Es necesario estar alerta ante ciertos síntomas y signos que pueden aparecer en el transcurso de una OM y que puedan hacer sospechar la complicación de un proceso otógeno.
Topográficamente se pueden diferenciar dos tipos de complicaciones, las intratemporales y las intracraneales, siendo estas últimas muchas veces consecuencia de las primeras.
Intratemporales:
– Mastoiditis.
– Laberintitis.
– Parálisis facial.
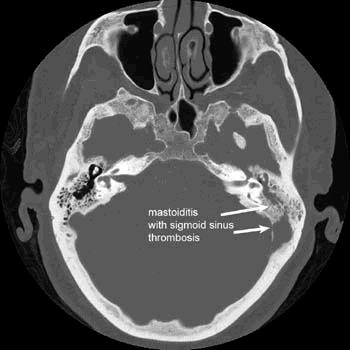
-Tromboflebitis del seno lateral.
-Petrositis.
En la era preantibiótica, la mastoiditis se presentaba en el 3-20 % de las OMA, actualmente podemos hablar de unas tasas de complicación de la OM del 2-0,24 %, e incluso hasta del 0,002 % en algunos países más desarrollados sanitariamente. El porcentaje de complicaciones intracraneales se sitúa en el momento actual entre el 0,24-0,36 %. La mortalidad es de algo más del 18 % en estos casos, y casi siempre se debe a un absceso temporal cerebral (31 %). El 0,45 % de las OMA supuradas pueden desarrollar una complicación extracraneal. La mortalidad global se debe, casi exclusivamente, a complicaciones intracraneales, y es próxima al 8 %.
ETIOLOGÍA.
El primer factor es el microorganismo productor de la infección, siendo un factor predisponente el tipo y virulencia del mismo.
Un tratamiento antibiótico inadecuado o insuficiente puede ser otro factor predisponente. Es importante la susceptibilidad que presente el germen con relación a los agentes quimioterápicos que se estén administrando para combatirle. En general, cuando se producen complicaciones de la OM, es raro encontrar casos en los que el paciente no esté tomando un antibiótico que generalmente es adecuado y suficiente, pero a pesar de lo cual surge la complicación. Lo que sí que influye es la eficacia que ese tratamiento tenga sobre la infección primaria.
Asociación de enfermedades sistémicas crónicas concomitantes: diabetes, alcoholismo, etc. En el diabético especialmente pueden producirse formas necróticas muy destructivas.
Los gérmenes responsables son los mismos que se encuentran en las infecciones timpanomastoideas: neumococo, estafilococo, proteus y estreptococo hemolítico. En las complicaciones de la OMC, por su flora frecuentemente polimicrobiana, se pueden encontrar además gramnegativos y anaerobios.
PATOGENIA.
La infección una vez establecida en el oído medio y en sus celdas comunicantes va a intentar extenderse por la vía de menor resistencia a las estructuras adyacentes o distantes. Una vez que el proceso inflamatorio ha desbordado la mucosa y se difunde más allá del revestimiento mucoperióstico del oído medio afecta al hueso y ya se ha producido una complicación, que se manifestará cuando se haya extendido lo suficiente como para producir síntomas clínicos.
Las infecciones agudas se propagan generalmente por vías preformadas o tromboflebitis, mientras que las crónicas suelen hacerlo por erosión ósea.
Vías de propagación:
– La erosión de las paredes óseas realizada sobre todo por el colesteatoma, con lo que la infección se extiende por contigüidad al córtex petromastoideo. Así ocurre por ejemplo en la OMA necrosante o en las OMC con osteitis y colesteatoma. Por este mismo mecanismo de contigüidad puede erosionarse el tegmen, la porción petrosa del temporal, el conducto de Falopio alcanzando el facial, el laberinto, el seno lateral o la dura madre. Este es el mecanismo por el que con más frecuencia se originan complicaciones en las supuraciones timpanomastoideas.
– Vías preformadas congénitas por alteraciones de desarrollo: suturas dehiscentes, bulbo de la yugular dehiscente, a través de la ventana oval o redonda, conexiones vasculares directas, fracturas craneales y soluciones de continuidad creadas quirúrgicamente. Todas estas vías facilitan la expansión de la infección al endocráneo.
– Vías preformadas adquiridas: fracturas, estapedectomía, etc.
– Osteotromboflebitis: por este mecanismo se pueden producir complicaciones en las OMA que puede manifestarse de forma precoz en pocos días.
Las complicaciones pueden aparecer cuando la infección se difunde más allá del revestimiento mucoperióstico del oído medio.
DIAGNOSTICO.
La clínica va a depender de la complicación que se trate.
En el momento actual, al tratarse de pacientes ya tratados con quimioterapia, la clínica suele ser muy solapada, enmascarada y de difícil diagnóstico. Pueden presentarse cuando la OM persiste más de dos semanas, cuando tras una remisión a las dos semanas aparece una recrudescencia del proceso infeccioso, cuando hay una exacerbación de una OMC, comienzo de otorrea fétida durante el tratamiento, cuando la infección es por Haemophilus Influenza tipo B o por anaerobios.
En la exploración son signos sospechosos de una complicación: fiebre asociada a OMC, desplazamiento del pabellón en una OM, dolor retro-orbital o parálisis facial del lado de la OM, aparición de vértigo o nistagmus en una OM, cefalea intensa, meningismo, papiledema, signos de focalidad neurológica.
El diagnóstico de estos procesos ha experimentado un vuelco total gracias a las nuevas técnicas de imagen, específicamente la tomografía computarizada (TC) y la resonancia magnética (RM). Una TC de alta resolución puede proporcionar fabulosas imágenes del estado del complejo tímpano-mastoideo y de muchas de las estructuras relacionadas
MASTOIDITIS
Es la osteitis de la apófisis mastoides manifestada exteriormente. Es decir, que solo cuando el proceso inflamatorio que tiene lugar en el interior de hueso se exteriorizase y se manifiesta mediante síntomas clínicos se diagnostica de mastoiditis, este es un concepto clásico pero actualmente mediante las imágenes TAC se pueden apreciar mastoiditis sospechadas pero que no se han evidenciado todavía de forma clínica mediante signos externos.
Esta complicación de la OM, como el resto de sus complicaciones, con el advenimiento de los antibióticos ha experimentado un notable descenso, llegando a ser rara, pero en ocasiones éstos no resuelven el proceso, lo que obliga al tratamiento quirúrgico de urgencia para evitar las temidas complicaciones endocranéales que ponen en peligro la vida del paciente. Es la complicación de origen otógeno más frecuente y puede manifestarse aislada o asociada a otras complicaciones más graves intra o extratemporales.
Proceso de neumatización de la mastoides.
El proceso de neumatización de la apófisis mastoides consiste en la formación de celdas aéreas en su interior y comienza a las pocas semanas antes del nacimiento para completarse antes del final del segundo año de vida.
A los seis meses el lactante existen celdas junto al antro. Pero la existencia de celdas mastoidea es muy variable en extensión y tamaño de unos individuos a otros y la causa de estas variaciones ha sido objeto de controversias y sigue siéndolo. No hay una explicación satisfactoria para el hecho de que un niño menor de un año pueda tener un sistema de celdas aéreas plenamente desarrollado, de forma que pueda requerir una intervención para el drenaje de un empiema agudo, mientras que un anciano puede tener una mastoides esclerótica sin celdas en la nunca se puede producir un empiema.
– El concepto ortodoxo es el de la reabsorción del hueso diplóico por la invasión activa de CC epiteliales, originadas den la caja del tímpano, como proceso vital responsable de la neumatización. Desde el antro, la invasión epitelial da origen a las celdas mastoideas y a las del antro. Las celdas mastoideas también pueden comunicar directamente con el oído medio por debajo del NF. Aunque la apófisis mastoides no se hace prominente hasta después del nacimiento, en la mayoría de los individuos el proceso de neumatización comienza antes de nacer. Esto es importante tenerlo en cuenta para comprender el papel de la otitis infantil en la detención del proceso de neumatización. Esta teoría esta respaldada por la evidencia.
– Otra teoría sobre la neumatización de la mastoides es la llamada mesodérmica. Según esta teoría el proceso de neumatización se produce de forma primaria en el mesodermo. Los espacios vacuolados corresponden a espacios medulares y la aireación sería debida a la rotura de los tabiques de separación de estos espacios.
– Teoría de la tracción sobre la mastoides. El crecimiento de la mastoides sería debido la tracción ejercida por sus inserciones musculares que produce una separación de las tablas óseas interna y externa. El aire entre en el espacio potencial así formado como simple resultado de la comunicación atmosférica que existe a través de la trompa de Eustaquio y el oído medio. Cuando esta vía de entrada de aire está bloqueada ello conllevaría una falta de neumatización.
– Hipótesis de Wittmaack (1918). La membrana mucosa que recubre la caja del tímpano es la responsable de la formación de las celdas mastoideas y así una mucosa normal produce un desarrollo normal de celdas mastoideas. Un estado patológico de esta mucosa puede ser debido a la entrada de meconio o de caseum epidérmico en el oído medio ó bien a las otitis del lactante. Cuando la mucosa es patológica se produce una inhibición parcial o total, o un retraso, en el proceso de neumatización quedando la mastoides con celdas pequeñas, escasas o incluso compacta ebúrnea.
Todas estas teorías pueden no ser exclusivas unas de otras, así la neumatización puede depender de la capacidad de las CC epiteliales tubotimpánicas de invadir el mesénquima como de la posibilidad de que entre aire en los espacios potenciales preformados. Igualmente parece posible que la capacidad invasora de las CC epiteliales puede verse dañada por la inflamación del oído medio en la infancia.
Etiología.
Esta complicación es más frecuente en la infancia y adolescencia si bien puede afectar a personas de todas las edades. 36-42 % de todos los casos de mastoiditis aguda se producen en menores de 2 años, lo más frecuente es que aparezcan entre los 6 meses y 3 años.
Se produce tras una OMA, o tras la reagudización de una OMC. La OMA se acompaña generalmente por contigüidad de una mastoiditis aguda transitoria que afecta a la mucosa en grado variable y que es reversible espontáneamente tras el tratamiento de la otitis, fenómeno conocido como mastoidismo y que no tiene manifestaciones clínicas evidentes de mastoiditis. De aquí que algunos autores hablan de timpanomastoiditis mas que de OM. Si la infección continua, aparecen osteoclastos con la producción de osteitis y reabsorción de trabéculas óseas que da lugar a la formación de espacios lacunares, constituyendo ya una mastoiditis. Es decir, la mastoiditis es la lesión inflamatoria que trasciende de la mucosa al hueso de los espacios óseos intercanaliculares.
Generalmente se trata de una infección monomicrobiana. Con frecuencia pueden aparecer estudios bacteriológicos negativos debido a que la acción de los antibióticos hace que estas lesiones queden abacterianas, o bien en las llamadas formas L de las bacterias que son difíciles de reconocer.
Los patógenos responsables son los mismos que los de la OMA:
– Neumococo (30%)
– Haemophilus influenzae (15%).
– Estreptococo beta hemolítico (15%).
– Estafilococo aureus (10%).
– Pseudomona auroginosa (4%).
– Otras gram (-).
Las infecciones virales pueden ser también las responsables de este proceso: la gripe sigue siendo uno de los virus con apetencia ótica. Las infecciones por virus de las enfermedades eruptivas infantiles siguen dando complicaciones en las otitis.
La mitad de los casos, o incluso más, tienen el antecedente de OMA, ahora bien, también están descritos otros factores asociados como la otitis sero-mucosa crónica (20 %), la adenoidectomía (30 %) y las malformaciones congénitas no otológicas (20 %).
Patogenia.
La vía patogénica más común es la de contigüidad por propagación de gérmenes a través de la mucosa desde la caja, trompa de Eustaquio o rinofaringe, a través del antro a la mastoides. En esta patogenia tiene una especial importancia el drenaje mastoideo. La OMA es yugulada con los antibióticos, pero queda en el interior de la caja y la mastoides una retención purulenta que tiende a espesarse y a organizarse. La inflamación de la mucosa antromastoidea, en especial la del espacio inter-ático-timpánico, o aditus ad antrum, puede impedir un correcto drenaje de esta secreción y dar lugar a un empiema.
La propagación por vía hemática, especialmente la venosa, puede explicar la patogenia de ciertos procesos mastoideos, en los que el posible foco de origen se encontraría en el seno esfenoidal y celdas etmoidales posteriores. La siembra en la mastoides por vía arterial de un germen circulante es el mecanismo productivo más común de todas las osteomielitis; esto tendrá más importancia cuanto más diploica y rica en médula ósea sea la mastoides.
Además de las causas infecciosas, en los traumatismos mastoideos, cada día más frecuentes, puede producirse por diversos mecanismos una mastoiditis aguda. En el traumatismo de la mastoides y el peñasco (fracturas longitudinales y oblicuas) se produce una comunicación de la caja y con el CAE y los gérmenes pasan entonces fácilmente a la mastoides. También puede originarse por la infección de hematomas postraumáticos dentro de la cavidad.
Anatomía patológica.
El proceso puede iniciarse en cualquier grupo de celdas mastoideas, si bien la mayoría de las veces se inicia en el antro, pero si la obstrucción del drenaje ocurre entre el antro mastoideo y las celdas de otros grupos, la mastoiditis se inicia en éstos.
La mastoiditis luego puede predominar en éste o aquel grupo de celdas, siempre buscando la expansión por donde el proceso infeccioso encuentre la menor resistencia.
El proceso tiene consecutivamente una fase congestiva, exudativa y osteítica. Se produce una inflamación de la mucosa con gran vasodilatación capilar, formación de pus, ulceración de la mucosa y destrucción por osteitis purulenta de los tabiques intercelulares fusionándose las celdas.
La intensa vasodilatación del mucoperiostio provoca la descalcificación rápida de estos finos tabiques que separan una celda de su vecina, lo que facilita a que el proceso inflamatorio encuentra libre el camino para invadir por contigüidad un grupo de celdas. La trombosis séptica de los capilares lleva a la necrosis séptica de zonas más o menos extensas de la mucosa y de elementos óseos. Su acumulación en el interior de la cavidad forma un absceso cerrado, fase de empiema mastoideo.
Casi siempre este proceso de ulceración mucosa, congestión intensa, infiltración pericapilar con trombosis y osteitis, tiene lugar en varios grupos de celdas a la vez, ello hace que puedan existir múltiples focos en una mastoiditis aguda. La asociación de un pequeño empiema con el vecino va acumulando en el interior de la mastoides cada vez más pus, que en algún punto alcanza la cortical mastoidea. La tendencia natural más frecuente es hacia delante, donde encontrará el CAE, y por encima del macizo facial y hacia fuera, donde se encontrará con la cortical externa de la mastoides.
La fusión de los grupos celulares periantrales, superficiales externos y posteriores, da lugar a la llegada de la colección a una zona cortical situada por encima de la inserción del músculo ECM y del esplenio. Si perfora la cortical, levanta el periostio en una zona situada por detrás y por encima del pabellón, el abombamiento de esta región extendiéndose hacia la zona zigomática es característico de las exteriorizaciones de una mastoiditis aguda, especialmente en la infancia.
La dirección de la colección purulenta del espacio intersinu-facial, junto con las celdas de la punta, da lugar a una exteriorización hacia la cortical de la punta de la mastoides.
Las características de la inflamación aguda de la mastoides van a depender fundamentalmente del tipo osteológico de la mastoides. Una mastoides neumática puede dar lugar a todas las eventualidades expuestas, no así en una mastoides ebúrnea o diploica. Este es el riesgo de la mastoides infantil en fase de neumatización, rica en zonas medulares, a través de las cuales se producen verdaderas osteomielitis que pueden llevar a invadir todo el peñasco.
Una mastoides es ebúrnea cuando el hueso diploico o esponjoso se hace ebúrneo. Los espacios mastoideos que se encuentran por fuera del antro y de las celdas yuxta-antrales profundas se condensan y en consecuencia se crea una fuerte barrera a la progresión hacia el exterior de una colección antral.
Junto a este prototipo de mastoiditis aguda existen otros casos en los que la virulencia del germen está atenuada, es decir, el binomio germen-defensas orgánicas se encuentra menos desnivelado que en el caso anterior. La inflamación del hueso en estos casos es de descalcificación y necrosis del foco, pero la osteogénesis entra en juego desde la periferia y en consecuencia al lado de fenómenos destructivos hay una tendencia regenerativa de tipo osteoblástico que tiende a rodear el proceso.
Existen por el contrario formas hiperagudas producidas por una fuerte virulencia del germen y una disminución de las defensas. Estas formas puede aparecer una mastoiditis inicial sin pasar por el periodo de la OMA. La osteomielitis del peñasco pertenece a este tipo de formas hiperaguda de extraordinaria gravedad.
Anatomopatológicamente se ha podido comprobar como los antibióticos, por su acción sobre los gérmenes causantes, pueden detener la necrosis tisular rápida y así pueden fomentarse los procesos de reparación. El hecho es que los focos de fusión no curan, sino que persisten a pesar del tratamiento con antibióticos. Esto podría explicarse porque en el seno avascular de un foco de destrucción, el medicamento no se administra a concentraciones suficientes y por ello no resulta fácil a este nivel una destrucción de los gérmenes.
Clínica.
El cuadro clínico puede aparecer en cualquier fase de la OM, pero especialmente en la fase de supuración o resolución, tras un período de aparente mejoría.
La sintomatología puede ser clara y evidente facilitando el diagnóstico, pero también hay casos de sintomatología larvada (mastoiditis enmascaradas o asintomáticas) mostrándose el proceso cuando ha dado ya lugar a una complicación endocraneal.)
Sintomatología:
– Dolor: puede no ser llamativo, aparece en una OMA en vías de curación y es menos intenso que el del la fase aguda de la otitis, si bien es la mayoría de los casos si que llama la atención siendo espontáneo, notándose en el fondo del oído con irradiación a mastoides y cráneo. Suele ser gravitatorio y con exacerbación nocturna.
Este dolor mastoideo se difunde a todo el hemicráneo. Las contracciones de los músculos de la mastoides, ECM, trapecio, digástrico, etc., son dolorosas y en consecuencia puede aparecer una tortícolis característica.
Si la formación del empiema es en las celdas perisinusales, el dolor se refiere situado en las zonas posteriores hacia la región occipital. Cuando la zona zigomática es la que se encuentra afectada predominantemente, los dolores tienen una localización e irradiación hacia la región temporomaxilar, los movimientos masticatorios se hacen cada vez más dolorosos.
– Cuando la otitis es supurada, la supuración aumenta, aunque en ocasiones puede no ser profusa por bloqueo del additus.
– Síntomas generales: aumento o reaparición de la fiebre, astenia, adinamia y empeoramiento del estado general. Empeoramiento de la audición y reaparición de otorrea. La fiebre puede tomar el aspecto de fiebre séptica en agujas. A veces en niños puede asociar signos de meningismo.
Exploración.
Es habitual que aparezca una tumefacción y un eritema en la región retroauricular, con edematización y borramiento del surco retroauricular (signo de Jacques) y antepulsión y despegamiento del pabellón auricular en mayor o menor grado. Edema de la pared póstero-superior del CAE. Este aspecto es debido a que el foco destructivo tiende a evacuarse hacia el exterior y el edema y la hinchazón desplazan el pabellón hacia delante. En los niños, pueden aparecer edemás palpebrales.
La palpación de la mastoides es cada vez más dolorosa, tiene su punto de máxima sensibilidad a nivel de la punta de la mastoides, en la zona del triángulo de Macewen.
Dentro del proceso de evacuación otro lugar de expansión que puede observarse como signo externo es el CAE, en estos casos se aprecia un engrosamiento de la pared posterior con estenosis de la luz. El descenso de la pared posterior del CAE puede ser un signo típico de mastoiditis. Cuando una otorrea persiste más de quince o veinte días sin tendencia a aumentar su contenido mucoso, siempre indica cierto grado de participación mastoidea. Ahora bien, en el momento actual la mastoiditis que se presenta en pacientes tratados con antibióticos, son muy frecuentes los casos en que no hay supuración y el tímpano está íntegro.
La imagen otoscopia puede ser similar a la de cualquier otra OMA con o sin perforación timpánica, pero si que puede mostrar además datos que son sospechosos de mastoiditis, ya que toda mastoiditis se acompaña de la inflamación de las paredes del aditus lo que pone de manifiesto por una desaparición del ángulo póstero-superior del surco timpanal. El abombamiento conjunto del tímpano y del surco timpanal es un signo precoz de las mastoiditis agudas. Luego el abombamiento se propagará a la pared póstero-superior del CAE. La otoscopia puede ser también totalmente normal y anodina.
Con la OMA aparece una hipoacusia de transmisión o conducción, la cual cede entre la segunda y tercera semana de evolución, pero si se complica con una mastoiditis ésta se hace más intensa. El Rinne es negativo y el Weber está lateralizado al lado afecto.
En la analítica aparecerá una leucocitosis con polinucleosis.
Diagnóstico.
Se realiza por:
– La clínica.
– La analítica muestra leucocitosis y polinucleosis con cayados abundantes y frecuentes granulaciones tóxicas en los leucocitos. VSG elevada.
– Las técnicas de imagen tienen especial interés y más en las formas enmascaradas, pues las imágenes van a definir y confirmar el diagnóstico. Rx simple de mastoides comparando ambos lados: en las radiografías simples se puede apreciar además del grado de neumatización, un flou o velamiento de la trabéculas óseas de la mastoides, incluso puede mostrar destrucción clara de trabéculas y formación de lagunas.
– TAC: es la prueba de elección ante la sospecha de una mastoiditis, tanto para confirmar las hipótesis diagnósticas como para evaluar la necesidad de tratamiento quirúrgico urgente y para el control evolutivo de la enfermedad. Muestra la opacidad de las celdas mastoideas y puede mostrar niveles hidroaéreos. Pueden aparecer lagunas en la región otoantral como signo que demuéstrala presencia de osteitis. Puede mostrar otras complicaciones intra y extratemporales.
En caso de sospecha de una complicación intracraneal, por presentar el paciente focalidad neurológica o disminución del estado de conciencia, la prueba de imagen más fiable es la RM. Así, podremos objetivar colecciones epi o subdurales, meningitis, tromboflebitis del seno venoso lateral e, incluso, abscesos cerebrales temporales. En estos infortunados casos, la RM será de gran valor de cara a la actitud terapéutica a tomar.
La posible existencia de un colesteatoma debe de estar siempre presente en una mastoiditis tanto en niños como en adultos.
Diagnóstico diferencial.
– No se debe confundir una mastoiditis con una adenopatía retroauricular inflamada en el contexto de una otitis o de una lesión infectada del cuero cabelludo, lo cual no es infrecuente. Una palpación cuidadosa, el contexto clínico e incluso las pruebas de imagen permiten diferenciarlo.
– En adolescentes e incluso en adultos, la sobreinfección de un quiste sebáceo retroauricular proporcionará una imagen de absceso, fluctuación y dolor, pero la ausencia de afección ótica asociada disipa las dudas.
– Una furunculosis del CAE puede producir una tumefacción de la porción cartilaginosa del conducto, pero no el hundimiento de la pared posterosuperior. De manera adicional, el tímpano y la caja no necesariamente resultarán afectadas en las enfermedades exclusivas del CAE.
Tratamiento.
Antibioterapia adecuada según la gravedad del cuadro a dosis suficientes y prolongadas. Estos corrigen los síntomas generales y locales, pero no pueden detener siempre el proceso destructivo mastoideo, sobre todo en caso de acción bacteriostática insuficiente. Se aconseja utilizar cefalosporinas de segunda o tercera generación por vía parenteral a dosis máximas y, más adelante, se revalorará el antibiótico en función del cultivo. El uso de corticoides no es generalizado pero alivia el dolor y disminuye la tumefacción e inflamación de una forma significativamente rápida. Se aconsejan ciclos cortos de metilprednisolona a dosis de 1-1,5 mg/kg/día. Algunos autores aconsejan los antinflamatorios.
Miringotomía con colocación de drenaje y toma de exudado para antibiograma: se aconseja realizarlo en todos los casos.
Con estas dos medidas la evolución suele ser muy favorable, siendo muy difícil que evoluciona a una mastoiditis supurada.
Cuando existe absceso subperióstico se debe de proceder primero a su aspiración postauricular con aguja, o bien directamente drenaje del mismo.
Hoy es raro tener que recurrir a la mastoidectomía cortical; es decir con conservación, si es posible, de la pared posterior del CAE y abordaje retroauricular. Se indica:
– Cuando el cuadro no cede y tiende a la cronificación.
– Cuando existe sospecha clínica de colesteatoma
– Cuando aparecen complicaciones supurativas extratemporales.
Evolución.
La evolución tratada precozmente es a la curación, tras la instauración del tratamiento antibiótico y paracentesis.
Puede evolucionar en compañía de cualquiera de las otras complicaciones extra y endocranéales de la OM. Cuando no cura, su evolución natural es hacia la exteriorización o la interiorización.
Uno de los factores de los que va a depender su evolución es de la edad. En las personas mayores la fistulización externa no suele producirse, pues en general evoluciona bajo el signo de la insensibilidad, siendo más frecuente una otorrea mucosa. La otorrea persistente en el adulto es siempre sospechosa de mastoiditis y es posible asistir a mastoiditis en las que el primer síntoma es precisamente la complicación endocraneal. En el lactante reviste peculiaridades que luego se exponen.
La evolución hacia la exteriorización puede manifestarse anatómicamente por diversas formas clínicas:
– Exteriorización retroauricular: es la vía más habitual. Se forma un absceso subperióstico primero en toda la zona de la inserción del músculos ECM y del esplenio, luego a través de la cortical externa por encima y detrás del CAE, forma un absceso retroauricular y posterior fistulización a piel. En estos casos el foco de fusión afecta al grupo celdas perisinusales, en especial las de la región posterior del seno lateral y la supuración sigue el camino de la vena emisaria mastoidea. Hay un borramiento del pliegue retroauricular y el PA es desplazado hacia adelante La evacuación de este absceso se realiza fácilmente.
– Exteriorización temporocigomática: se produce debido a la existencia de celdas en la raíz posterior del zigoma, están conexionadas con el antro mastoideo a través del ático y de las celdas intralaberínticas. Se producen con más frecuencia en el individuo joven La fusión con fistulización subperióstica provoca el desplazamiento del pabellón auricular hacia fuera, abajo y hacia delante. Puede llegar a formarse un absceso en la cara superficial del músculo temporal. La tumefacción de los párpados puede ser muy aparatosa y puede plantear el diagnóstico diferencial con una etmoiditis acompañada de una oftalmía fluxionaria, si bien pueden coincidir ambos procesos. La invasión de la articulación TNM provoca fuertes dolores al mover la mandíbula.
La cigomatitis puede confundirse fácilmente con una parotiditis. El contexto clínico, la otoscopia y las pruebas de imagen serán de gran utilidad en estos casos poco frecuentes.
– Absceso de Luc: es la producción de una osteitis en la pared posterior del CAE y drenaje hacia éste produciendo la denominada fístula de Gelle. Puede confundirse con una otitis externa abscesificada, pero tanto la función auditiva como las pruebas de imagen proporcionarán su confirmación.
– Fistulizaciones posterosuperiores. La colección purulenta se forma bajo la aponeurosis epicraneal. Son responsables las celdas yuxtasinusales, en el ángulo posterosuperior de la mastoides. El dolor está localizado en la zona correspondiente a las celdas de Citelli y es característico el empastamiento doloroso de esta zona. Estas celdas se relacionan por detrás con la fosa cerebelosa y el seno lateral, por arriba con la fosa cerebral media y por delante con las celdas peri-antrales que llevan al antro mastoideo, por lo que en consecuencia la fistulización externa es el accidente más favorable que puede ocurrir.
– Mastoiditis o absceso de Bezold. Se produce la erosión de la cortical interna del ápex mastoideo con la formación de una colección supurada entre el músculo ECM y digástrico. La infección puede seguir la arteria occipital y a través de las fascias y vainas musculares cervicales, alcanzar los grandes vasos del cuello apareciendo una tumefacción laterocervical con síntomas y signos cervicales. Teniendo en cuenta que la neumatización de la punta de la mastoides no se ha desarrollado en el niño, se comprende que este tipo de mastoiditis sea raro en la primera infancia, si bien a partir de los nueve o diez años ya pueden presentarse este tipo de mastoiditis. Aparece tortícolis. Su tratamiento es quirúrgico de drenaje, debiendo de realizarse una mastoidectomía ampliada hasta la punta de la mastoides.
– Mastoiditis de Seudo-Bezold. Es más frecuente que la anterior y consiste en una exteriorización de la infección a nivel de la región apical externa de la mastoides en la inserción del ECM con miositis de éste y formación de una colección purulenta. Es consecuencia de una osteitis de las celdas del espacio intersinu-facial de Traube, siendo el grupo superficial de las mismas el que sirve de camino para alcanzar la cortical externa. Aparece además una tortícolis. El tratamiento consiste en la mastoidectomía y drenaje del absceso.
– Mastoiditis yugulodigástrica de Mouret (o de Duhnn-Mouret). Su presentación actualmente es excepcional. Consiste en la formación de una colección purulenta profunda, debajo del músculo digástrico, en el espacio retroestíleo. Se produce por la fusión de los grupos profundos de celdas subantrales de Mouret, por dentro de la ranura digástrica, lo que hace que su fistulización inferior quede coleccionada en un espacio formado por esta masa muscular, la aponeurosis cervical media por fuera y la pared faríngea por dentro. Estas formaciones purulentas representan, en principio, un absceso parafaríngeo, situado por detrás del pilar posterior de la amígdala palatina. Ocupan el espacio retroestíleo del cuello en contacto con la carótida interna y con la yugular. En la clínica se asocian síntomas faríngeos como trismus y odinofagia. En la exploración se aprecia un abombamiento visible de la parea lateral de la faringe. También puede exteriorizarse hacia la región occipital. El signo de Luc, consiste en un aumento de la otorrea cuando se ejerce una presión en la región cervical y suele ser positivo y de gran valor diagnóstico. La colección purulenta queda muy cerca de la apófisis trasversa de las vértebras cervicales por lo que la intensidad de los dolores por compresión inflamatoria de las raíces de los nervios intervertebrales es considerable y en esta situación cualquier movimiento de la columna cervical despierta intensos dolores. Casi siempre conlleva una meningitis de la fosa posterior.
– Osteomielitis aguda de la mastoides. Es una afección rara, puede darse en la infancia y especialmente en el lactante. En estas edades es posible la osteomielitis difusa de la mastoides en las formas muy graves, que llevan a la muerte y pueden pasar inadvertidas. Puede ocurrir cuando una OMA es causada por un germen de gran virulencia puede lesionar la caja, el aditus y el antro, creando una lesión en cavidad cerrada. Es posible que al ulcerarse la mucosa, la supuración se ponga en contacto con los espacios medulares, lo que significa la posibilidad de difusión fácil y rápida. Es más frecuente en la infancia y en el lactante, con escasa neumatización y rico contenido medular del hueso.
El germen causal es casi siempre el estafilococo sin embargo se han encontrado otros gérmenes como el estreptococo y neumococo.
La osteomielitis tiene una fase de principio brusco, con intensas algias temporales, occipitales y zigomáticas, gran quebrantamiento general con fiebre en agujas y fuertes escalofríos. El empastamiento de la mastoides se hace aparente desde el comienzo de la otitis, la extensión del empastamiento hacia la región cervical o submaxilar es signo de gravedad.
La aparición de complicaciones pulmonares concomitantes puede ocurrir y es debido a la abundante comunicación venosa de la medula ósea del peñasco y la mastoides, lo cual hace que sea posible la llegada de micro émbolos sépticos al pulmón.
Las complicaciones de la mastoiditis hacia el interior son la petrositis, la laberintitis, la parálisis facial y las complicaciones endocranéales.
PARALISIS FACIAL
Es una complicación intrapetrosa de la OMA y sobre todo de la OMC, especialmente de la colesteatomatosa. La lesión causal asiente en el oído medio y se extiende secundariamente al trayecto intratemporal del nervio facial. Se trata de una PF unilateral que va precedida siempre de una inflamación del oído medio y que en ocasiones acompaña a otras complicaciones intratemporales de la OM, tales como mastoiditis, laberintitis, etc.
En el momento actual es muy poco frecuente debido a una serie de razones:
* Diagnóstico precoz de las OMA y OMC tanto por el pediatra como por el otólogo, lo que supone la instauración igualmente precoz de tratamiento.
* Eficacia terapéutica de los quimioterápicos, antibióticos y antinflamatorios, tanto de acción tópica como por vía parenteral.
* Progresos de la cirugía funcional del oído que permite sin riesgo acciones terapéuticas y diagnósticas inmediatas, incluso en lactantes.
* Por estas razones hoy en día la PF otógena no supone más del 1 ó 2% de las PF.
Etiología y patogenia.
La patogenia más clara ocurre en la OMC colesteatomatosa: el conducto de Falopio es erosionado por la masa colesteatomatosa o por tejido de granulación produciendo una lesión nerviosa.
En las OMA se precisa como condición previa una solución de continuidad del conducto de Falopio ya sea congénita o adquirida.
Para que los gérmenes productores de una otitis media lleguen a producir una parálisis facial además de su presencia y patogenicidad se requieren otros factores, tales como una virulencia exacerbada.
Otros factores que pueden influir en esta complicación son una predisposición anatómica constitucional del oído, alteraciones en la respuesta tisular y enfermedades generales concomitantes como agammaglobulinemias, HIV, diabetes, etc.
El oído del niño pequeño y del lactante es más vulnerable a esta complicación, ya que no ha concluido su desarrollo y en su osificación existen todavía dehiscencias fisiológicas del canal óseo de Falopio así como comunicaciones vasculares entre su contenido y la mucosa que tapiza el oído medio.
Se ha comunicado que existen factores constitucionales y familiares que explican la frecuente aparición de otitis media recidivante en gran número de los miembros de una misma familia, así como la incidencia de complicaciones otógenas de diverso tipo de los mismos. No se conoce si es una predisposición heredada, ya que no se han demostrado cuales son los factores genéticos implicados en esta transmisión hereditaria (estado inmunológico, factores anatómicos, etc.). Se ha apuntado a que la causa puede estar en compartir los mismos factores ambientales por toda la familia.
Los mecanismos de producción de la parálisis facial otógena se pueden resumir en tres que pueden actuar aisladamente o complementándose entre sí:
– Edema tóxico de la vaina neural.
– Neuritis infecciosa.
– Compresión extrínseca.
El edema tóxico de la vaina neural es un mecanismo que casi solo puede producirse en el lactante o en el niño muy pequeño. Es debido a que las toxinas bacterianas y otras sustancias liberadas por el propio tejido inflamatorio alcanzan rápidamente la vaina neural del nervio facial a través de las soluciones de continuidad y deshiscencias del canal óseo o de los vasos comunicantes antes citados. Este edema de la vaina se propaga a lo largo del canal y determina una compresión intrínseca de las fibras nerviosas. El edema del perineuro aumenta el contenido frente a un continente de paredes óseas inextensible. Este mecanismo de producción de la parálisis facial es el principal responsable de la misma en las OMA no supuradas sin apenas sintomatología otoscópica y de muy precoz aparición.
La neuritis infecciosa resulta de la participación del canal óseo del facial y de su contenido nervioso en el proceso supurativo, y a menudo necrosante, del oído medio. Este tipo de parálisis facial se presenta casi siempre en las OMA supuradas y necrosantes, especialmente como epifenómeno de las enfermedades infecciosas de la infancia. Hoy por fortuna su frecuencia ha disminuido ostensiblemente. También puede producirse en las reagudizaciones o recalentamientos de una OMC, sobre todo, si existen lesiones mucosas y óseas graves. Estas agudizaciones, con la subsiguiente exaltación de la virulencia de los gérmenes causales, se presentan tras un proceso de tipo catarral de las vías aerodigestivas superiores y por la reinfección del oído medio a través de la perforación timpánica, sea por los baños estivales en piscinas, sea por la penetración de irritantes químicos o cuerpos extraños a través del CAE. En cualquier caso se produce la invasión del conducto de Falopio por exudados inflamatorios, gérmenes piógenos, elementos celulares conjuntivos migratorios, etc., frente a los que reacciona el perineuro con vasodilatación, edema y hasta necrosis de sus elementos celulares y fibrilares. Estas lesiones y la compresión intrínseca por el edema determinan el bloqueo funcional de las fibras nerviosas y su desmielinización. Este tipo de parálisis aparece tras varios días de evolución de la OMA y OMC reagudizada.
La compresión extrínseca del nervio facial es propia de la OMC con colesteatoma. Se produce tanto por una osteitis como por microabscesos subperiósticos y granulaciones conjuntivo-vasculares que comprimen extrínsecamente al nervio. El colesteatoma destruye las paredes óseas por presión y por la actividad enzimática y osteoclástica que posee en su matriz. De esta forma acaba por irrumpir en el interior del canal facial comprimiéndolo e inflamándolo. Este tipo de paralisis otógena se desarrolla muy lentamente en el transcurso de meses o años. Casi nunca aparece de forma inesperada, como cuando es resultado de otros tipos de OMA, sino que se manifiesta en portadores de otorreas crónicas con largo historial clínico en los que las complicaciones, y entre ellas la PF, ya había sido vaticinada por el otólogo con anterioridad.
Sintomatología.
La parálisis facial suele comenzar por una paresia y además este tipo de parálisis no suele afectar a todas las ramas por igual y su intensidad puede fluctuar a lo largo de horas o de días. No suelen afectarse las ramas sensitivo-sensoriales.
La coexistencia de otitis media jamás falta en la parálisis otógena. La aparición súbita de una paralisis sin antecedentes otíticos puede plantear problemas de diagnóstico diferencial sobre todo con la paralisis facial idiopatica, pero la anamnesis bien realizada, suele descubrir la existencia previa a la parálisis de un cuadro catarral de vías altas con alteraciones del estado general y sobre todo otalgia pulsátil o hipoacusia subjetiva homolaterales. La consignación de tales datos es difícil en niños y lactantes.
La reaparición de la supuración de un oído que ya supuraba anteriormente, o el aumento de la otorrea, unido a otalgia intensa y a hipoacusia en OMC, precediendo todo ello a la parálisis y tras un resfriado de vías altas o los baños estivales tienen una significación inequívoca. En estas situaciones, la reactivación de la OMC ha conducido inexorablemente a la complicación intratemporal y a la parálisis.
La otoscopia es otro elemento del diagnóstico de confirmación y de diagnóstico diferencial. Generalmente se trata de un oído perforado con otorrea, pudiendo observarse o no escamas, granulomas y casi siempre se puede apreciar una gran inflamación de la mucosa.
Hipoacusia de conducción más o menos acentuada dependiendo de las lesiones mucosas y óseas concomitantes que se confirma mediante audiometría. Cuando con la paralisis coexiste una laberintitis, la hipoacusia se hace mixta, de manera que suele existir una hipoacusia de conducción para los tonos graves y un predominio del componente de percepción para los tonos agudos. Suelen asociarse al cuadro acúfenos de tono grave y desequilibrio-vértigos. La equilibración muestra una lateralización con caída hacia el lado enfermo manifiesta en el Romberg y en la prueba de brazos extendidos. En las fases de mayor actividad del proceso inflamatorio aparece un nistagmus espontáneo horizonto-rotatorio que bate hacia el lado sano en armonía con la desviación del tronco y de los miembros. Se trata de un nistagmus espontáneo de origen vestibular periférico y de tipo deficitario.
En otras ocasiones no existen signos vestibulares manifiestos, pero los pacientes se quejan de mareos, de inestabilidad momentánea y repetida, y de estado nauseoso más o menos pertinaz. En estos casos, la maniobra de Lucae puede revelar la aparición de un nistagmo provocado por la presión positiva o negativa con la pera de Politzer en el CAE. Dicho cambio de presión se transmite al laberinto posterior a través de la solución de continuidad de su pared ósea y desencadena un nistagmus, como en la clásica experiencia de Ewald: signo de la fístula positivo.
No obstante, la clínica de la paralisis otógena varía según la edad, la etiología y patogenia y la coexistencia con otras complicaciones intratemporales o intracraneales de la otitis. Su pronóstico y su tratamiento son asimismo distintos. De ahí que convenga estudiar por separado las diferentes formas clínicas conocidas.
Paralisis facial otógena precoz en OMA.
Se trata casi siempre de una paralisis facial unilateral, súbita e inesperada, que aparece en lactantes o niños muy pequeños en las primeras 12 o 24 horas de evolución de una OMA, pudiendo ser incluso el síntoma revelador de la misma.
Tras un cuadro prodrómico de coriza y catarro de vías aerodigestivas superiores con fiebre, malestar general, rinorrea mucosa o mucopurulenta, tos irritativa e inapetencia, surge un cuadro clínico de OMA con otalgia, inquietud motora, desasosiego, llanto, vómitos, diarreas, etc. que rápidamente se acompaña de paralisis facial unilateral de tipo periférico. El oído puede supurar o no, si bien la parálisis suele preceder a la supuración.
Otras veces, tras este cuadro prodrómico surge la paralisis y es al explorar al paciente para esclarecer la etiología de dicha parálisis cuando se descubre la OM.
Es una paralisis facial unilateral y homolateral, de tipo periférico, en las que se afectan los músculos inervados por las dos ramas, si bien suele estar más afectados los bucales que los frontales. La parálisis casi nunca suele ser completa, de manera que más que parálisis hay una paresia de la musculatura. Suele ser muy intensa al principio para remitir total o parcialmente con fluctuaciones en el momento de iniciarse la otorrea. Ello es debido a que la salida de exudados a través de la perforación timpánica conlleva una reducción importante de la presión ejercida sobre el nervio por los exudados a tensión del oído medio.
No suele existir afectación de las fibras sensitivas ni sensoriales gustativas del NF, como tampoco de las parasimpáticas secretoras destinadas a la glándula lagrimal.
Paralisis Facial en las OMA y OMC reagudizadas.
En la actualidad este tipo de paralisis facial otógena sólo se observa en la práctica como complicación de una OMC agudizada. Antes de la época antibiótica aparecía en el trascurso evolutivo en las OMA exudativas hipervirulentas y necrosantes, especialmente en las enfermedades infecciosas de la infancia.
Hoy en día, tales formas clínicas de las OMA han pasado casi por completo a la historia gracias al empleo precoz y normalmente acertado de antibióticos por parte del pediatra o médico generalista, de tal forma que se evitan la Tromboflebitis del seno lateral s lesiones mucosas y óseas destructivas del oído medio y se previenen las complicaciones.
Únicamente se sigue observando la paralisis facial otógena en la evolución de las OMA viriásicas gripales, pero aquí puede discutirse el origen otógeno de dichas PF. En efecto, la lesión nerviosa se produce en estas OM por las hemorragias capilares en el interior del Falopio, con la subsiguiente compresión intrínseca del nervio, así como la propia inflamación del nervio por el virus neurotropo gripal. Sólo la infección secundaria por gérmenes piógenos a través de la perforación timpánica o de la trompa, sería en ocasiones la responsable de la osteitis del canal y de la lesión secundaria del NF.
En las OMC de perforación marginal con lesiones mucosas tales como granulaciones y pólipos y con lesiones óseas a nivel de la cadena osicular y del propio canal del nervio facial, sobre todo en su trayecto timpánico, en las que suceden los fenómenos de destrucción y reparación tisular, puede presentarse una paralisis tras una agudización o recalentamiento de la otitis. Con menor frecuencia sucede esto en OMC con perforación central o en las perforaciones inactivas.
Sea por la reinfección del oído medio a través de la perforación, como ocurren en los baños de piscina, sea por la penetración de un cuerpo extraño, o sea por la reactivación del proceso a través de la trompa, tras un resfriado o catarro de vías altas, un brote de adenoides en los niños, etc., se produce un aumento de la supuración del oído, la proliferación de conjuntivo-vascular y en definitiva la otitis. Tras varios días de evolución, con supuración abundante, hipoacusia y otalgia manifiesta, surge la PF en el lado afecto con características similares a las descritas en las formas anteriores. Se trata de una peresia por afectación motora del NF, sin alteraciones secretoras, sensitivas ni gustativas.
La parálisis no surge inmediatamente, sino tras un período variable de evolución entre una y tres semanas. A diferencia de la forma antes descrita, predominan aquí los síntomas locales otológicos sobre los generales.
Paralisis facial otógena en las OMC colesteatomatosas.
De todas las formas clínicas de PF otógenas es ésta la que se presenta con mayor frecuencia y gravedad. Se trata de una parálisis que surge en portadores de OMC de perforación marginal, con colesteatomas que ocupan y destruyen el epitímpano y la mastoides, y que por presión, usura y osteolisis enzimática de la cortical ósea acaban por destruir la pared ósea del canal facial e irrumpen en su interior. Además de la presión mecánica sobre el nervio, comportan una inflamación más o menos circunscrita del mismo, responsable del edema y de la parálisis. Esto suele ocurrir en los puntos en los que el canal de Falopio es menos grueso y más superficial, es decir, a nivel de su porción timpánica, por encima del nicho de la ventana oval y del promontorio, y por debajo del CSE. Así se explica la coexistencia frecuente de una fístula de dicho conducto, a partir de la cual se presenta una laberintitis crónica circunscrita de evolución lenta y con sintomatología vertiginosa recidivante.
La Paralisis facial puede surgir espontáneamente en el curso evolutivo de esta OM colesteatomatosa. Otras veces aparece tras una reactivación de la supuración por los baños en mar y piscinas, o tras manipulaciones intempestivas de limpieza del oído medio. Los síntomas configuran un cuadro clínico serio y alarmante. Hay otalgia espontánea, que aumenta por la presión sobre la mastoides, localizada en la región ótica y periótica y que se irradia con carácter pulsátil hacia la región temporal homónima. La supuración densa, fétida, pardusca y a veces hemorrágica, suele acompañarse de la presencia de escamas epidérmicas. La hipoacusia suele ser intensa y manifiesta. Con frecuencia la paralisis va precedida o acompañada de un cuadro de vértigo rotatorio con náuseas y vómitos, con inestabilidad que inmoviliza al paciente en el lecho y como broche final surge la PF, contrastando este cuadro local grave con una sintomatología general anodina o inexistente.
OMC agudizada, laberintitis y PF unidas configuran el cuadro clínico habitual. Este cuadro puede presentarse también en pacientes sin historia de OMC en los que se ha desarrollado un colesteatoma retrotimpánico, o en enfermos operados de timpanoplastia y en los que por detrás de un neotímpano aparentemente sano se ha reproducido el colesteatoma a expensa de restos de matriz insuficientemente eliminada.
Diagnóstico.
El diagnóstico se obtendrá a partir de la anamnesis, paciente con PF de rápida evolución ipsolateral al cuadro de una OM.
Para la confirmación de la sospecha clínica se realizará un TAC, en el que puede llegar a observarse la dehiscencia.
Pronóstico.
Si el origen es una OMA, se recuperará sin grandes defectos la movilidad facial normal, siempre que se siga un tratamiento adecuado.
En las parálisis faciales por procesos crónicos o colesteatomatosos, que son los más habituales, la recuperación es más difícil, pero mediante una cirugía de urgencia es posible, en algunos casos, recuperar la movilidad de manera progresiva.
Tratamiento.
Dependerá de su etiología, patogenia, gravedad y de la posible coexistencia con otras complicaciones intratemporales.
Siempre se comienza por antibioterapia por vía parenteral (con cultivo y antibiograma, si es posible) y antinflamatorios de tipo esteroideo.
Si no hay perforación timpánica se ha de realizar una paracentesis a nivel del cuadrante anteroinferior con drenaje de exudados.
En las crónicas se realiza una limpieza exhaustiva de secreción con toma de muestra de exudados para estudio bacteriológico.
Cuando la causa es una OMC colesteatomatosa la indicación quirúrgica es absoluta siendo las alternativas quirúrgicas múltiples y dependiendo de la gravedad y extensión de las lesiones. En la mayoría de los casos se trata de amplios colesteatomas que destruyen por completo la caja del tímpano, al antro y la mastoides, originan una fístula del CSE y finalmente abren en mayor o menor medida el canal óseo del facial. En tales casos se realiza una radical de oído medio con amplia comunicación de la cavidad mastoidea con el exterior a través de la caja y CAE unida a una descompresión quirúrgica de la segunda y tercera porción del NF.
En casos de lesiones menores y más circunscritas se realiza exéresis de las lesiones con descompresión del facial pero debe de intentarse conservar parte o la totalidad de la cadena osicular, pudiendo incluso realizar reconstrucción de cadena en el mismo tiempo quirúrgico.
LABERINTITIS.
Se trata de la inflamación de la región laberíntica en el contexto de un proceso infeccioso agudo o crónico del oído medio. Puede aparecer como consecuencia de OMA, de OMC colesteatomatosa, o tras la cirugía del oído. Además de la etiología otógena, la laberintitis puede tener su etiología en una meningitis cerebroespinal o piógena (laberintitis meningógena), en una infección por vía hemática y en traumatismos accidentales o quirúrgicos.
LABERINTITIS CIRCUNSCRIPTA.
También conocida como laberintitis crónica, perilaberintitis, o fístula laberíntica. Se ha de diferenciar de la fístula perilinfática postraumática de la ventana oval .Esta afección es específica de la otitis media colesteatomatosa y se produce por erosión de la cápsula ótica del laberinto con exposición del endosito e irritación laberíntica. Su lugar de asentamiento más frecuente es en la eminencia ósea del canal semicircular externo (CSE), situada en el antro mastoideo, pero también puede localizarse en el resto de los canales y en el promontorio. La erosión da lugar a una fístula entre la cavidad timpánica y la luz laberíntica.
Clínica.
Episodios fugaces de vértigo y nistagmo espontáneo que se desencadena con cualquier maniobra que aumente la presión en el oído medio: movimientos, manipulación del oído, etc.
Hipoacusia de transmisión debida a la patología causal.
A la exploración se aprecian los signos de la infección otológica. Signo de la fístula positivo: nistagmo hacia el lado patológico al ejercer una presión positiva sobre el oído colesteatomatoso.
El diagnóstico se realiza mediante los datos clínicos y la exploración mediante TC.
Tratamiento.
Siempre quirúrgico del proceso causal: timpanoplastia con exéresis completa del colesteatoma.
El pronóstico es bueno, siempre que se extirpe el colesteatoma y una vez se haya compensado la sintomatología vertiginosa.
LABERINTITIS SEROSA.
También denominada laberintitis aguda toxica.
Se trata de una inflamación intralaberíntica difusa y reversible, total o parcialmente, producida por una reacción inflamatoria de vecindad, es decir, un proceso agudo o crónico en el oído medio.
Etiología.
Puede estar producida por OMA y más raramente por OMC. Es muy típica la que se produce postestapedectomía y la de la otitis de la escarlatina.
Patogenía.
Existe paso de toxinas y factores de la inflamación hacia el laberinto produciendo la consiguiente irritación del mismo. La penetración se produce a través del ligamento anular de la ventana oval o de la membrana de la ventana redonda.
Se produce en primer lugar una dilatación y aumento de la permeabilidad capilar de la red subaratnoidea del espacio endolaberíntico y perilinfático, cerca del lugar de la invasión al laberinto. Esto va a traer como consecuencia un aumento de la presión en los líquidos laberintos, produciéndose un hidrops. La hiperpresión produce una deformación de los elementos endoteliales sin destruirlos, aunque pueden estar intensamente alterados.
El paciente sufrirá, además del cuadro vertiginoso, una hipoacusia con la posibilidad de resolverse con tratamiento.
Anatomía patológica.
No se ha constatado más que una congestión de los vasos y la presencia en los líquidos laberintos de finos depósitos de fibrina.
Clínica.
Vértigo moderado con nistagmo espontáneo hacia el lado de la lesión, es decir, hacia el oído con el proceso otítico.
Hipoacusia neurosensorial moderada.
Evolución.
Suele ser un proceso reversible con recuperación funcional.
Tratamiento.
Respecto al tratamiento, se utilizarán antibióticos por vía parenteral, corticoides, sedantes vestibulares y, en caso de existir un colesteatoma, éste deberá intervenirse quirúrgicamente. Si el proceso desencadenante es una OM se realizará una timpanocentesis y colocación de un drenaje temporal.
Si no cede, o se trata de una infección crónica: mastoidectomía y laberintectomía en casos de cofosis.
LABERINTITIS SUPURADA.
También denominada aguda supurada, destructiva o necrosante. Invasión de los espacios laberínticos por bacterias y cc inflamatorias con presencia de pus y detritus.
Se trata de un proceso muy serio que en su evolución natural conlleva la anulación irreversible del laberinto y que cursa con un síndrome vertiginoso acusado e hipoacusia aguda no reversible.
Etiología.
OMA y OMC. Mastoiditis. Meningitis.
La infección se propaga desde el oído medio al laberinto por una osteitis que llega a producir efracción ósea que lo más frecuente es que sea por erosión del CSE y más raramente a través de las ventanas o del promontorio.
También puede propagarse si efracción ósea a través del ligamento de la platina del estribo.
Se ha descrito algún caso sin lesión parietal ni penetración microbiana, siendo la patogenia totalmente oscura a falta de una constatación anatómica.
Clínica.
Se caracteriza por la aparición, en un paciente aquejado de un proceso ótico previo, de crisis vertiginosas e hipoacusia. Los acúfenos pueden o no estar presentes. Es una clínica de estado grave. Los vértigos son violentos y acompañados de intensa sintomatología vegetativa. Hipoacusia profunda o cofosis. Frecuente asociación de complicaciones endocranéales.
Aparece un nistagmo en la exploración que es de tipo ablativo, paralítico o de destrucción, es decir, hacia el lado sano, hacia el oído no afectado.
Evolución.
La resolución de la inflamación es lo más frecuente que acarree daño permanente por fibrosis y neoformación ósea (laberintitis osificante).
Muchos autores afirman que no es posible diferenciar entre una laberintitis serosa de una supurada hasta valorar el estado cócleo-vestibular a posteriori, es decir, si existe o no reversibilidad en la audición.
Aunque raro, puede evolucionar a una difusión endocraneal de la infección, originando una meningitis o un absceso endocraneal.
Tratamiento.
Antibióticos.
Quirúrgico en caso de:
– OMA sin respuesta al tratamiento o aparecen complicaciones endocranéales.
– OMC. No debe de realizar laberintectomía en caso de que quede algún resto auditivo.
– Timpanoplastia, si existe colesteatoma.
TROMBOFLEBITIS DE LOS SENOS VENOSOS ENDOCRANÉALES.
La rica red venosa del oído medio está en comunicación directa con varios senos venosos intracraneales y en particular con el seno lateral. La riqueza de anastomosis entre los senos y venas cerebrales y la carencia de válvulas explican las posibilidades de difusión de estas complicaciones venosas. La tromboflebitis más importante y frecuente es la del seno lateral.
Este tipo de complicaciones ha disminuido mucho en nuestro tiempo, sobre todo en el curso de las otomastoiditis agudas, pero sigue presentándose de tanto en tanto en las OM osteítico-colesteatomatosas reactivadas.
La más frecuente es la del seno lateral pudiendo también producirse en el resto de los senos de la duramadre más raramente.
TROMBOSIS DEL SENO LATERAL.
En la OMC colesteatomatosa se produce por un mecanismo de periflebitis. Bien puede producirse al afectarse la pared del seno lateral alojado en un canal del macizo petromastoideo y en íntimo contacto con las celdillas, o bien porque la inflamación llega por continuidad a lo largo del sistema venoso desde las vénulas de la mucosa o desde la vena emisaria mastoidea.
Sintomatología.
Al estar el paciente bajo el efecto antibiótico, su presentación suele presentar aspectos que hace difícil determinar si se trata de un cuadro septicémico o una tomboflebitis. En la época preantibiótica los signos septicémicos eran evidentes y gravísimos.
Naturalmente, cuando la sepsis acontece en el curso de una OMA supurada o sigue a la exacerbación de una OMC, es difícil pensar en la tromboflebitis como causa de dicha septicemia. En estos casos son ciertos signos locales los que pueden orientar a contemplar tal eventualidad: empastamiento y dolor espontáneo o a la presión en la región mastoidea. Cuando la mastoides está afectada de un modo difuso, la sintomatología séptica puede aparecer en cualquier momento del curso de la infección. Si la mastoiditis tiene un curso subagudo, los signos de afectación del seno lateral pueden aparecer en la tercera a quinta semanas. Pero en la actualidad, bajo el efecto antibiótico, estos cuadros siguen un curso más solapado y todas estas manifestaciones clínicas aparecen tardíamente y con muy pocos síntomas.
Ahora bien, si los síntomas de sepsis (escalofríos, fiebre en agujas, cefalea, deshidratación, leucocitosis, hemocultivo positivo, etc) aparecen durante una OMC sin reactivación, el diagnóstico será mucho más difícil. En estos caso si no se puede encontrar otra causa de la sepsis, deberíamos sospechar una OMC colesteatomatosa que ha afectado por erosión el seno lateral. El examen sistemático del oído puede revelar su responsbilidad. Precisamente en la actualidad es muy frecuente ver esta afección como un hallazgo operatorio, particularmente en los casos producidos por neumococo. La intervención pone de relieve que la infección se ha producido por contigüidad con lesiones de osteitis y periflebitis que alcanza el seno.
Pueden existir signos de irritación meníngea pero sobre todo es importante observar el estado cansado y afectado del enfermo. Un aspecto serosanguinolento del fluido de la otorrea puede indicar una inflamación aguda necrosante timpanomastoidea. La otorrea espesa puede también indicar un proceso erosivo mastoideo.
La caída de la pared posterosuperior del conducto óseo y el empastamiento retroauricular señalan la posible existencia de un empiema mastoideo. La fluctuación en la zona retroauricular correspondiente a la vena emisaria es un signo a favor de tromboflebitis de esta vena. La fluctuación del borde anterior del ECM en su parte alta o el infarto ganglionar también en este punto pueden indicar tromboflebitis del golfo de la yugular. Lo habitual es no encontrar estasis papilar, si existe puede ser en uno o en ambos ojos, de grado variable, pero más marcado en el lado afecto. En tales casos hay que suponer la extensión a los otros senos. Mediante la prueba de Crowe-Beck pueden sacarse conclusiones de gran valor, en condiciones normales, cuando se comprimen ambas yugulares en el cuello se provoca una notable estasis venosa intracraneal que se aprecia oftalmoscópicamente por dilatación de las venas retinianas o a simple vista de las venas faciales. Si entonces deja de comprimirse una de ellas, tal estasis desaparece al existir intercomunicación de ambos sistemas venosos, pero si existe obstrucción unilateral por tromboflebitis del seno lateral, al liberar dicho lado, no cede la estasis.
En los tratados antiguos se hacia hincapié en un signo patonogmónico: al estar ocluido el sistema yugulo-cavernoso no aumenta la presión del LCR al comprimir las yugulares.
El resto del examen neurológico es normal. Las pruebas de imagen hoy son definitivas para el diagnóstico.
Analíticamente se puede apreciar una importante leucocitosis y neutropenia.
La evolución del proceso si no se trata es grave por la posibilidad del fenómeno tromboembólico hacia los otros senos endocranéales por arriba, hacia la yugular por abajo, por embolización séptica hacia el pulmón o por extensión endocraneal meningitis abscesos, etc. Con la antibioterapia han disminuido extraordinariamente estos peligros y ha mejorado su pronóstico.
Tratamiento.
La mayoría de los autores consideran que es demasiado esperar que los antibióticos erradiquen los foscos de infección mastoideos, por lo que es imperativo hacerlo quirúrgicamente. El tratamiento quirúrgico está clásicamente bien establecido: amplia mastoidectomía en casos de otomastoiditis aguda, realizando exanteración de todas las celdillas enfermas o mastoidectomía a la demanda en los casos de OMC. En ambos caso se procede a la exposición del seno, extirpando la cortical ósea antero-externa que lo recubre desde el ángulo de Citelli por arriba hasta el golfo de la yugular por abajo, eliminando con ello todas las lesiones perisinusales. A continuación, la punción en diversos puntos nos permite apreciar sitio y grado de obstrucción venosa, absceso intrasinusal, etc, para curetear en ambos sentidos hasta llegar al fin de la zona obstruida. Se aconseja dejar la herida abierta.
TROMBOSIS SENO CAVERNOSO.
La trombosis del seno cavernoso es la obstrucción trombótica del seno, generalmente causada por la diseminación de bacterias a partir de la infección de un seno paranasal, áreas perisinusales y más raramente a partir de OM. Cuando es de origen otógeno casi siempre va precedida de trombosis del seno lateral apareciendo como una complicación más de la misma.
Otra posible origen es una trombosis retrograda a partir de una trombosis del seno petroso o de los plexos carotídeos. También puede originarse por contigüidad de una infección del apéx petroso.
Clínica.
Cursa con dolor orbitario que aumenta con la presión sobre el globo ocular, equimosis conjuntival, exoftalmos, oftalmoplejía ipsilateral que puede hacerse bilateral y afección de la rama oftálmica del trigémino, puede llegar a la oftalmoplegia completa. Es frecuente la presencia de fiebre, rigidez nucal, ectasia de las venas retinianas y papiledema.
Si el cuadro es importante puede aparecer equimosis palpebral y exoftalmos.
PETROSITIS.
La denominación de petrositis para los procesos inflamatorios, crónicos o agudos, del peñasco, y especialmente de su punta, fue propuesta en 1935 por Kopetky y Almour mediante la publicación de un trabajo en el que presentaban 10 casos. Hasta entonces no había una denominación unánime y segura y de ahí los diferentes nombres que ha recibido este proceso, como osteitis profunda, roqueitis, osteomielitis, síndrome del peñasco, etc.
Etiopatogenía.
El factor etiológico originario es una OM. La llegada de un proceso supurativo a la pirámide petrosa se produce, por fortuna, menos frecuentemente de lo que pudiera sospecharse. Las vías de acceso de la infección a la punta del peñasco son la vía ósea y la venosa.
Los gérmenes aislados más frecuentes, valorando la casuística de diversos autores, son: Estreptococo, Neumococo y E. Coli. El estreptococo es el que está presente con mayor frecuencia, con diferencia sobre el resto de los gérmenes.
La estructura de la pirámide petrosa es el factor local más importante. La complicación es tanto más fácil que se produzca cuanto mayor sea la neumatización de peñasco. La pirámide se encuentra neumatizada en un porcentaje reducido de casos. Se comprende que un hueso ebúrneo, sin celdas neumáticas, es prácticamente imposible que sea lesionado por una colección purulenta procedente de la caja del tímpano, ya que su progresión es ir avanzando de espacio en espacio celular.
Además del hueso neumático, el hueso diplóico, propio de las pirámides infantiles, es otro de los tipos que pueden dar facilidades a la progresión de una colección purulenta desde el antro mastoideo al ático o a la caja del tímpano, por el camino de los espacios medulares.
El diferente tipo de la neumatización de la pirámide petrosa tiene por tanto una influencia decisiva en la aparición, o no, de una petrositis. Es más frecuentes en la infancia, a expensad de mastoides diplóicas, siguiendo los espacios medulares. En los adultos serán más propensos aquellos con mastoides muy neumáticas.
Existen tres vías óseas que corresponden a las tres caras de la pirámide:
• La vía superior, está representada por las celdas de las cadenas supra-trans-retrolaberínticas. Alcanza la punta del peñasco por la cresta de la pirámide, pasando por encima del CAI. Es la más larga de las tres vías.
• Vía anterior. Está formada por las cadenas precoclear e inter-carótido-coclear. Llega al ápex por el espacio comprendido entre la carótida y la parte superior del bloque laberíntico. Es la vía más corta.
• Vía inferior, integrada por las cadenas de celdas infralaberínticas, de donde parte hacia la punta, discurriendo entre la cóclea, la carótida, el acueducto de la cóclea, el CAI y el golfo de la yugular.
Ahora bien, también se han descrito casos en pacientes con temporales ebúrneos y en tales casos la diseminación de la infección es directa desde el proceso agudo del oído medio, tratándose en estos casos de una verdadera osteomielitis.
En cuanto a la vía venosa, fue Pietrantoni quién investigando la patógena del Síndrome de Gradenigo, demostró que esta vía participaba en este proceso, al comunicar con la punta de la pirámide venas de la caja. Las vénulas de la caja tienen anastomosis con otras que las ponen en relación con lo senos petrosos superior e inferior, pudiendo conducir así la infección hacia el VI par y al seno cavernoso. El plexo venoso carotídeo también puede formar parte de esta vía.
Las enfermedades carenciales y metabólicas pueden igualmente influir como factores predisponentes en la aparición de una petrositis.
El sexo ha sido estudiado como factor predisponente, pero los resultados son muy discordantes.
Edad: más frecuente en el niño que en el adulto.
Además de la OM, la OE en su forma de OE maligna puede alcanzar el peñasco por diversas vías. Esta infección que comienza en el CAE puede provocar una erosión directa de la mastoides, del oído medio y finalmente llegar por esta vía hasta el peñasco.
Anatomía patológica.
Depende del tipo de neumatización que presente la pirámide. Teniendo en cuenta que el tejido ebúrneo prácticamente no existe en el ápex, sólo nos quedan dos tipos de neumatización, que son la neumática y la diplóica. Cuando la neumatización es de tipo neumático, la evolución del proceso inflamatorio será hacia la osteitis, mientras que cuando sea el diplóico, la evolución será hacia la osteomielitis.
Clínica.
Es muy frecuente que el cuadro debute con los síntomas de una septicemia, escalofríos, fiebre séptica y mal estado general. En los niños es frecuente que además se asocien síntomas gastrointestinales, pulmonares o meníngeos.
Lo más típico es que el cuadro presenta una tríada sintomática que ha quedado como clásica: OM, dolor y parálisis del VI par. La mayoría de los casos asocian síntomas mastoideos.
En general se trata de una OMA. La OMC rara vez evoluciona a una petrositis. La OM por colesteatoma en algunas ocasiones puede ser causa predisponente a la petrositis.
El dolor está presente casi siempre revistiendo las más variadas formas, siendo frecuentes las localizaciones parieto-temporales y las óculo-orbitales. Otra característica es su intensidad, ya que pueden ser atroces y lancinantes en unas ocasiones y más soportables en otras, pueden tener remisiones o ser constantes, localizados aquí o irradiados allá. En términos generales se pueden dar como características de este dolor su persistencia e intensidad.
La parálisis del VI par es un signo de los más importantes dentro de la tríada característica de la petrositis. La parálisis o paresia se presenta bajo el aspecto de estrabismo interno acompañado de diplopia. La parálisis se presenta de un solo lado, el mismo que corresponde a la lesión en el oído medio, aunque se encuentra también comúnmente en el lado opuesto o en ambos a la vez. Un dato muy importante a reseñar es que una petrositis puede iniciarse simplemente por la aparición de esta parálisis, por tanto la parálisis del VI par aislada debe hacer pensar inmediatamente en la posibilidad de una petrositis.
Al lado de esta tríada sintomática hay otro síntoma de orden general que puede presentarse en el trascurso del proceso:
• Fiebre de 38-39º C.
• Hemograma con una leucocitosis alta.
• Signo de Scheibe.
• Edema de papila por tromboflebitis del seno cavernoso.
Radiología.
La sospecha de una petrositis hace indicar la realización inmediata de un TAC o RM. Ambas técnicas muestran imágenes de celdillas neumáticas opacificadas y generalmente hay un engrosamiento de la duramadre sobre la punta del peñasco. Este engrosamiento suele extenderse al seno cavernoso, a través del punto donde se encuentra el conducto de Dorello y explica la parálisis del VI par. En la RM no se ven las paredes de las celdillas, pero con el TAC pueden observarse con frecuencia desmineralización de sus paredes.
Se han diferenciados dos tipos radiológicos de petrositis:
• Petrositis con ausencia de anomalía en la pirámide petrosa: la afectación apical está excluida, sin embargo, no podemos descartar que exista afectación perilaberíntica.
• Petrositis con anomalías de la pirámide petrosa: destrucción de celdas y trabéculas, veladura de la punta del ápex, alteraciones del reborde superior del ápex (fosita de Gasser).
Diagnostico.
Cuando se presenta con la sintomatología florida, un estudio radiológico confirma el proceso, y el diagnóstico no ofrece ninguna dificultad.
Ahora bien, en ausencia de alguno de sus tres signos característicos o cuando las imágenes radiológicas no son concluyentes, el diagnóstico es mas difícil.
Ante una OMA de dos a cuatro semanas de evolución, que comienzo con dolores del tipo señalado anteriormente, aunque no haya parálisis del VI par, siempre ha de estar presenta la posibilidad de una petrositis y lo mismo ocurre en la parálisis aislada del VI par.
Evolución.
En general es de naturaleza benigna, presentándose dicha evolución en tres períodos:
– El primero o congestivo, se caracteriza por los fenómenos dolorosos.
– El segundo o de supuración, en el que se establece el proceso inflamatorio osteoconjuntivo.
– El tercero, o terminal, con aparición de necrosis en el ápex y de complicaciones por ruptura ósea o diseminación hematógena.
Pronóstico.
Generalmente benigno, dependiendo de la localización y la virulencia del proceso inflamatorio, así como de la presencia o no de complicaciones.
Puede dar lugar a complicaciones endocranéales.
Tratamiento.
Antibioterapia y antinflamatorios precozmente y de forma persistente, hasta su remisión total. Es importante hacer cultivo para antibiograma.
Si el cuadro no evoluciona favorablemente es necesario realizar cirugía. Puede plantearse una mastoidectomía o una radical timpanomastoidea. En caso de que el cuadro adquiera una gran extensión se realiza el abordaje de Lampart entre la colea, la trompa de Eustaquio y la carótida interna. Hay que drenar la colección y extirpar el hueso enfermo, dejando la cirugía funcional para un segundo tiempo.
CONCLUSIÓN
Ante todo lo expuesto, es importante que:
Investiguemos con detenimiento los signos y síntomas de las patologías que derivan en estas complicaciones, ya que la falta de conocimiento de los mismos, el uso indiscriminado de antibióticos y la resistencia de los gérmenes a los mismos no nos permiten llegar a un abordaje diagnostico y terapéutico adecuado.
Tener también en cuenta la población, nivel socioeconómico bajo, alcoholismo, drogadicción, desocupación, que influyen en el fracaso o el incumplimiento de un tratamiento adecuado de las patologías de base aumentando así la aparición de sus complicaciones.
Actualmente contamos con estudios diagnósticos avanzados con ser las TAC y la RNM que nos ayudan a llegar con presicion a un diagnostico certero y así instaurar la terapéutica mas apropiada.
Imágenes
BIBLIOGRAFÍA.
– Cohen-Kerem R, Uri N, et al. Acute mastoiditis in children: Is surgical treatment necessary? J Laryngol Otol 1999; 113: 1081-5.
– Kaplan SL, Mason EO, PhD J: Pneumococcal mastoiditis in children [In Process Citation]. Pediatrics 2000 Oct; 106(4): 695-9
– Kvestad E, Kvaerner KJ, Mair IW: Acute mastoiditis: predictors for surgery. Int J Pediatr Otorhinolaryngol 2000 Apr 15; 52(2): 149-55
– Go C, Bernstein JM, de Jong AL, Sulek M, Friedman EM. Intracranial complications of acute mastoiditis. Int J Pediatr Otorhinolaryngol 2000;52:143-8
– Arístegui, Denia. Estado actual del diagnóstico y tratamiento de la mastoiditis en la infancia. En: Barberán MT, Sprekelsen MB, editores. Tratado de otorrinolaringología pediátrica. Ponencia Oficial SEORL, 2000; p. 141-50.
– Franco, Diogo, Franco, Talita, Gonçalves, Luiz Fernando Fernandes et al. Retalhos de gálea para fístulas de mastóide. Rev. Bras. Otorrinolaringol 2001;67:852-857.
– Bittencourt, Sérgio, Ribeiro, Ulisses J., Vichi Jr., Paulo A. S. et al. Flebite de seios sigmóide e tranverso & mastoidite de Bezold: relato de caso e revisão da literatura. Rev. Bras. Otorrinolaringol 2002;68:744-748.
– Katz A, Leibovitz E, Greenberg D, et al: Acute mastoiditis in Southern Israel: a twelve year retrospective study (1990 through 2001). Pediatr Infect Dis J 2003; 22: 878-883.
– Mustafa A, Debry Ch, Wiorowski M, Martin E, Gentine A. Treatment of acute mastoiditis: report of 31 cases over a ten year period.Rev Laryngol Otol Rhinol (Bord). 2004;125:165-9.
– Taylor MF, Berkowitz RG. Ann Otol Rhinol Laryngol 2004;113:69-72.
– Nussinovitch M, Yoeli R, Elishkevitz K, Varsano I. Acute mastoiditis in children: epidemiologic, clinical, microbiologic, and therapeutic aspects over past years.Clin Pediatr (Phila). 2004;43(3):261-7.
– Rathbun KC, Kendall MS. Mastoiditis in an immunocompetent adult South Med J. 2005; 98:577-8
– Minotti AM, Kountakis SE. Management of abducens palsy in patients with petrositis. Ann Otol Rhinol Laryngol. 1999;108:897-902.
– Al-Ammar AY. Recurrent temporal petrositis. J Laryngol Otol. 2001;115(4):316-8.
– Cudennec Y, Poucet JL, Verdalle P, Buffe P. Complications locoregionales des otites. Encycl Méd Chir: Otorhinolaryngologie 2005;20-135-A-10. Paris: Elsevier.
– Boenninghaus HG.. Otorrinolaringología. 9.ª ed. Barcelona: Ed. Springer-Verlag Ibérica, 1995.
– Ibáñez E, Juanola E, Liern C.. Complicaciones de las otitis. Manual del Residente ORL y Patología Cervicofacial 2002;I: 693-701.
– Becker W, Naumann HH, Rudolf PC. Otorrinolaringología. Barcelona. Ed. Mosby/Doyma, 1992. Boenninghaus HG. Otorrinolaringología. 9.ª ed. Barcelona: Ed. Springer-Verlag Ibérica, 1995.
– Quesada, Pumarola, López, Quesada. Complicaciones de las otitis medias. En: Barberán MT, Sprekelsen MB, editores. Tratado de otorrinolaringología pediátrica. Ponencia Oficial SEORL, 2000; p. 653-63.
Head Neck Surg 1998;124:1353-6.
– Bartomeus F. Supuraciones encefálicas otogenas, En: Abelló P, Traserra J, editores. Barcelona: Ediciones Doyma, S.A., 1992; p. 176-80.
– Kangsanarak J, Navacharoen N, Fooanant S, Ruckphaopunt K. Intracranial complications of suppurative otitis media: 13 years’ experience. Am J Otol 1995;16:104-9.
– Magliulo G, Terranova G, Cristofari P, Ronzoni R Sigmoid sinus thrombosis and imaging techniques. Ann Otol Rhinol Laryngol 1996; 105: 991993.
– Davison S, Facer G, McGough P, McCaffrey T, Reder P Use of resonance imaging and magnetic resonance angiography in diagnosis of sigmoid sinus thrombosis. Ear Nose Throat J 1997; 76: 436441
– Kurien M, Job A, Mathew J, Cahndy M. Otogenic intracranial abscess: Concurrent craniotomy and mastoidectomy changing trends in a developing country. Arch Otolaryngol Head Neck Surg 1998;124:1353-6.
– Bosch J, Rovira A, ÁlvarezSabín J, Capellades S, Abilleira S, Sumalla J Valor de la RM craneal en el seguimiento de las trombosis de senos durales. Rev Neurol 1998; 26: 971973.
– García RD, Baker AS, Cunningham MJ, Veber AL. Lateral sinus thrombosis presenting with extracranial head and neck abscesses. J Laryngol Otol 1994;108:779-82.
– Landsberg R, Lang R, Wollach B, Dubin Z, Ophir D. Lateral sinus thrombophlebitis. Harefuah 1994;126:386-9 y 427.
– Dennis R, García J, Mhsa MD, Baker S, Cunningham MJ, Alfred L et al Lateral sinus thrombosis associated with otitis media and mastoiditis in children. Pediatr Infect Dis J 1995;14: 617623.
– Delbrouck C, Mansbach L, Blondiau P Otogenic thrombosis of the lateral sinus: report of a case in a child. Acta Otorhinolaryngolog Belg 1996;50: 221226.